Nội dung chính
- 1. Đặt vấn đề
- 2. Bản chất di truyền phân tử của gen FUT2 và trạng thái tiết
- 3. Tương tác giữa trạng thái tiết và hệ vi sinh vật âm đạo
- 4. Vai trò của các loài Lactobacillus bảo vệ và sự tiến hóa của phân loại học
- 5. Cơ chế phân tử của nhiễm trùng ngược dòng và phản ứng viêm
- 6. Sự hiệp đồng giữa kiểu gen FUT2 và diễn tiến sinh non
- 7. Vai trò của Oligosaccharide (HMOs) và cân bằng nội môi chuyển hóa
- 8. Thách thức trong chẩn đoán và tầm nhìn y học cá thể hóa
- 9. Kết luận
- Tài liệu tham khảo:
Sinh non (preterm birth - PTB) được định nghĩa là sự chuyển dạ xảy ra trước 37 tuần tuổi thai, đây là một trong những thách thức dai dẳng nhất của linh vực sản khoa hiện nay. Theo ước tính toàn cầu, mỗi năm có khoảng 15 triệu trẻ sinh non chào đời cùng với các biến chứng liên quan là nguyên nhân hàng đầu gây tử vong ở trẻ em dưới 5 tuổi [1]. Sinh non không chỉ là một sự kiện lâm sàng đơn thuần mà còn là kết quả cuối cùng của một quá trình bệnh lý phức tạp, nơi các yếu tố di truyền, miễn dịch và vi sinh vật hội tụ. Trong nhiều thập kỷ, nhiễm trùng ngược dòng được xác định là nguyên nhân hàng đầu dẫn đến chuyển dạ sớm thầm lặng. Tuy nhiên, sự biến thiên trong kết cục lâm sàng giữa các cá thể có cùng tình trạng loạn khuẩn âm đạo đã đặt ra nhu cầu cấp thiết về việc tìm kiếm các yếu tố di truyền điều phối của vật chủ [2].
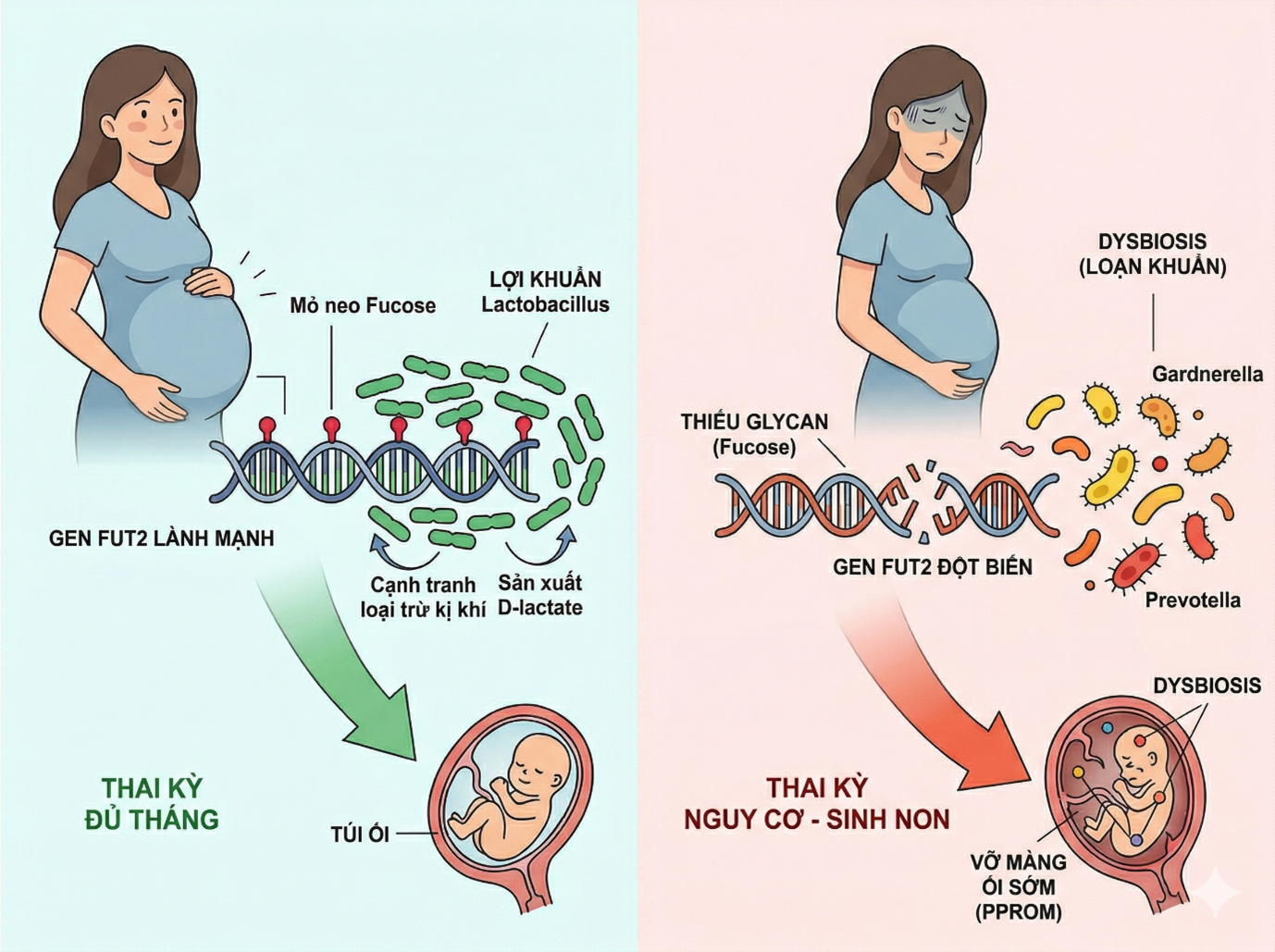
Gen FUT2 nổi lên như một yếu tố then chốt trong vấn đề này, nó quy định nguồn dinh dưỡng và khả năng bám dính của vi khuẩn thông qua cơ chế glycosyl hóa. Bằng cách mã hóa enzyme quyết định sự hiện diện của các kháng nguyên nhóm máu mô (Histo-Blood Group Antigens - HBGA) trên bề mặt niêm mạc, FUT2 đóng vai trò là "kiến trúc sư" thiết lập môi trường hóa học tại âm đạo. Sự tương tác giữa các glycan do vật chủ tiết ra và cộng đồng vi sinh vật không chỉ dừng lại ở mức độ cư trú mà còn can thiệp sâu vào các con đường tín hiệu viêm, từ đó quyết định tính toàn vẹn của màng ối và cổ tử cung trong suốt thai kỳ.
Gen FUT2 (Fucosyltransferase 2) nằm trên nhiễm sắc thể 19q13.3, mã hóa cho enzyme a(1,2)-fucosyltransferase. Enzyme này hoạt động trong bộ máy Golgi của tế bào biểu mô niêm mạc, xúc tác phản ứng gắn một phân tử đường L-fucose vào vị trí carbon số 2 của gốc galactose đầu tận cùng trên các chuỗi tiền chất oligosaccharide (hay còn gọi là glycan) (thường là chuỗi loại 1) [3]. Sản phẩm của phản ứng này là cấu trúc kháng nguyên H (H antigen). Kháng nguyên H là tiền thân để tạo ra các kháng nguyên nhóm máu A và B trong dịch tiết. Quan trọng hơn, tại niêm mạc âm đạo, các chuỗi glycan chứa fucose này đóng hai vai trò sinh học sống còn:
-
Nguồn dinh dưỡng (Prebiotic): Fucose là một nguồn carbon "cao cấp" mà chỉ những vi khuẩn đã thích nghi (co-evolved) như L. crispatus mới có bộ máy enzyme để sử dụng hiệu quả.
-
Thụ thể bám dính (Adhesion receptor): Các cấu trúc fucosyl hóa đóng vai trò là "mỏ neo", giúp lợi khuẩn bám trụ vững chắc vào biểu mô, chống lại dòng chảy rửa trôi của dịch âm đạo [4].
Trong quần thể người, sự đa hình di truyền của FUT2 dẫn đến hai kiểu hình rõ rệt.
-
Nhóm Tiết (Secretors - chiếm khoảng 80%) là những người mang ít nhất một alen FUT2 chức năng (Se/Se hoặc Se/se), cho phép biểu hiện glycan trên bề mặt niêm mạc âm đạo, tạo ra một môi trường giàu fucose máu hòa tan vào dịch tiết âm đạo hoặc sữa mẹ và thuận lợi cho L. crispatus phát triển [5].
-
Ngược lại, nhóm "Không Tiết" (Non-secretors - chiếm khoảng 20%) mang các đột biến vô nghĩa (nonsense mutations), phổ biến nhất là G428A (rs601338), dẫn đến enzyme bị mất chức năng hoàn toàn. Việc thiếu vắng fucose trên bề mặt niêm mạc âm đạo ở Nhóm không tiết không chỉ làm thay đổi đặc tính lý hóa của lớp chất nhầy mà còn làm mất đi các vị trí gắn kết tự nhiên của hệ vi sinh vật tại chỗ, tạo tiền đề cho sự mất cân bằng sinh học diễn ra nhanh chóng hơn [6–8].
Hệ vi sinh vật âm đạo khỏe mạnh ở phụ nữ trong độ tuổi sinh sản thường được đặc trưng bởi sự thống trị của các loài Lactobacillus. Trạng thái này được duy trì thông qua một cơ chế hiệp đồng tinh vi với vật chủ. Các kháng nguyên nhóm máu mô (HBGA) do FUT2 quy định hoạt động như những "mỏ neo" sinh học. Nhiều chủng Lactobacillus đã tiến hóa các protein bám dính đặc hiệu có khả năng nhận diện và liên kết với gốc fucose trên bề mặt biểu mô. Sự liên kết này giúp vi khuẩn duy trì vị trí cư trú ổn định trước cơ chế rửa trôi tự nhiên của dịch tiết âm đạo [6,8].
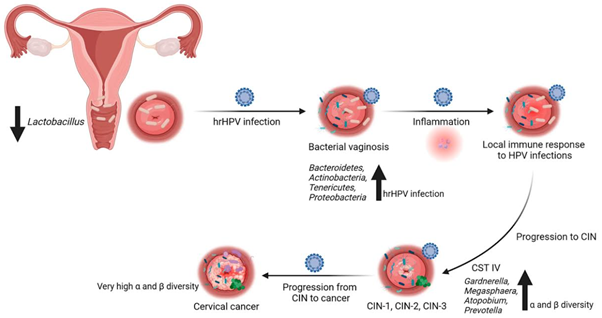
Hơn thế nữa, các fucose-glycan còn đóng vai trò là nguồn carbon chọn lọc. Quá trình lên men các carbohydrate này bởi Lactobacillus tạo ra axit lactic, giúp duy trì độ pH âm đạo ở mức axit thấp (pH < 4,5), từ đó ức chế sự phát triển của mầm bệnh. Ở Nhóm không tiết, sự vắng mặt của fucose tạo ra một "khoảng trống sinh thái". Hệ vi sinh vật ở nhóm này thường có tính đa dạng cao hơn nhưng lại thiếu ổn định, dễ chuyển dịch sang trạng thái community state type IV (CST IV) – trạng thái cạn kiệt lợi khuẩn và giàu vi khuẩn kị khí. Điều này cho thấy FUT2 không chỉ quyết định sự hiện diện của vi khuẩn mà còn là nhân tố duy trì khả năng phục hồi (resilience) của hệ sinh thái âm đạo trước các tác nhân gây nhiễu từ bên ngoài [8,9].
Sự hiểu biết về VMB đã tiến hóa vượt bậc nhờ vào giải trình tự metagenomics, cho phép chúng ta phân biệt vai trò của từng loài Lactobacillus ở cấp độ chủng. Lactobacillus crispatus (CST I) được xác định là loài bảo vệ ưu việt nhất đối với thai kỳ. Loài này sở hữu cụm gen mã hóa protein bám dính mucin (MucBP) và khả năng sản xuất D-lactate [10]. Khác với L-lactate, D-lactate có khả năng điều hòa miễn dịch tại chỗ và ức chế các enzyme matrix metalloproteinases (MMPs) hiệu quả hơn, giúp bảo vệ cấu trúc cổ tử cung [11].
Các nghiên cứu gần đây cũng đã tái phân loại các loài quan trọng khác: L. jensenii được xác định lại là Lactobacillus mulieris và L. gasseri là Lactobacillus paragasseri. Những loài này cùng với L. crispatus hình thành nhóm "vệ binh" chuyên biệt, sản xuất các axit amin N-acetyl hóa (như N-acetylserine) có tính kháng khuẩn mạnh mẽ. Ngược lại, Lactobacillus iners (CST III) lại mang đặc tính của một kẻ cơ hội. Với bộ gen tối giản, L. iners thiếu các gen sản xuất D-lactate và MucBP, khiến nó không thể tạo ra hàng rào bảo vệ vững chắc. Sự thống trị của L. iners thường là dấu hiệu báo trước cho một tình trạng loạn khuẩn có thể dẫn đến nhiễm trùng ngược dòng [10,11].
Nhiễm trùng ngược dòng là một diễn tiến sinh học có hệ thống. Khi các loài Lactobacillus bảo vệ bị suy giảm, các vi khuẩn mầm bệnh (pathobionts) như Gardnerella vaginalis, Atopobium vaginae và Prevotella bắt đầu tăng sinh. Chúng sử dụng các enzyme như sialidase và prolidase để phân giải nút nhầy bảo vệ cổ tử cung (cervical mucus plug), vốn là hàng rào cơ học ngăn cách âm đạo và bên trong tử cung [11].
Sau khi phá vỡ hàng rào cổ tử cung, vi khuẩn xâm nhập vào khoang tử cung và tiếp xúc với màng rụng (decidua). Tại đây, các mẫu phân tử liên quan đến mầm bệnh (PAMPs), điển hình là lipopolysaccharide (LPS), liên kết với các thụ thể Toll-like (đặc biệt là TLR4) trên bề mặt tế bào biểu mô và đại thực bào [11]. Sự liên kết này kích hoạt con đường tín hiệu NF-κB, dẫn đến việc sản xuất và giải phóng ồ ạt các cytokine tiền viêm như IL-1β, IL-6, TNF-α, và IL-8. Trong đó, IL-8 đóng vai trò then chốt trong việc huy động bạch cầu trung tính đến vị trí nhiễm trùng, tạo ra một ổ viêm khu trú nhưng có sức tàn phá mạnh mẽ đối với các mô liên kết xung quanh [12].
Điểm cốt lõi trong diễn tiến sinh non là sự kết hợp giữa đột biến vô nghĩa của gen FUT2 (tạo ra kiểu hình "Nhóm không tiết") và tình trạng loạn khuẩn âm đạo (thiếu hụt Lactobacillus). Tính chất nghiêm trọng của sự nhiễm trùng bị điều chỉnh trực tiếp bởi trạng thái tiết của vật chủ. Ở Nhóm tiết, các HBGA tự do trong dịch nhầy cổ tử cung hoạt động như các "thụ thể mồi nhử" (decoy receptors). Chúng liên kết với mầm bệnh, ngăn cản vi khuẩn bám vào biểu mô thật sự và giúp đào thải mầm bệnh ra ngoài. Nhóm không tiết hoàn toàn thiếu cơ chế bảo vệ từ xa này. Nghiên cứu trên nhóm phụ nữ mang thai cho thấy trạng thái không tiết là một yếu tố nguy cơ độc lập đối với việc rút ngắn thời gian mang thai khi kết hợp với sự thay đổi hệ vi sinh vật:[8]
|
Nhóm đối tượng |
Trạng thái vi sinh vật |
Thời gian mang thai trung bình (ngày) |
|
Nhóm không tiết |
Loạn khuẩn: Nhiều vi khuẩn đa dạng, ít Lactobacillus |
241,54 (nguy cơ cao) |
|
Nhóm không tiết |
Trội Lactobacillus |
266,21 |
|
Nhóm tiết |
Suy giảm Lactobacillus |
266,05 |
|
Nhóm tiết |
Trội Lactobacillus |
262,52 |
Dữ liệu cho thấy ở những nhóm không tiết, việc thiếu hụt vi khuẩn Lactobacillus trong giai đoạn sớm của thai kỳ dẫn đến thời gian mang thai ngắn hơn đáng kể so với các nhóm còn lại.
Kết quả là ở những phụ nữ không tiết, mầm bệnh có thể tiếp cận trực tiếp các thụ thể TLR (Toll-like receptor) trên bề mặt biểu mô một cách nhanh chóng hơn. Sự khuếch đại phản ứng viêm ở nhóm này diễn ra quyết liệt hơn, dẫn đến việc sản xuất các enzyme MMP (đặc biệt là MMP-2 và MMP-9) với nồng độ cao. Các enzyme này cắt đứt các sợi collagen trong màng ối và cổ tử cung, gây ra tình trạng chín muồi cổ tử cung sớm và vỡ ối sớm (Preterm Premature Rupture of Membranes - PPROM) [11]. Bằng chứng lâm sàng đã xác nhận rằng phụ nữ không tiết bị loạn khuẩn vào đầu thai kỳ có nguy cơ sinh non tự phát tăng gấp nhiều lần, với chiều dài thai kỳ bị rút ngắn trung bình từ 2 đến 3 tuần so với nhóm có gen tiết [8].
Sự tương tác giữa FUT2 và vi sinh vật còn được thể hiện qua các oligosaccharide tương tự như trong sữa mẹ (Human Milk Oligosaccharides – HMOs) hiện diện tại dịch tiết âm đạo. Các phân tử như 2'-fucosyllactose (2'-FL) – sản phẩm trực tiếp của enzyme do FUT2 mã hóa – đóng vai trò là chất điều hòa miễn dịch và là thức ăn ưu tiên cho các lợi khuẩn. 2'-FL có khả năng ức chế sự bám dính của các tác nhân nguy hiểm như liên cầu khuẩn nhóm B (Group B Streptococcus - GBS), một trong những mầm bệnh hàng đầu gây nhiễm trùng sơ sinh và sinh non [3,13].
Ngoài ra, các chất chuyển hóa như phenyllactate và indolelactate được sản xuất bởi hệ vi sinh khỏe mạnh cũng đóng góp vào việc duy trì cân bằng nội môi. Chúng hoạt động như những chất kháng nấm và kháng khuẩn tự nhiên, giữ cho quần thể vi sinh vật luôn ở trạng thái cân bằng [14]. Việc thiếu hụt FUT2 gián tiếp làm nghèo nàn hoạt động chuyển hóa này, khiến môi trường âm đạo trở nên "khô khan" và dễ bị tổn thương trước sự xâm nhiễm của các loài kị khí sinh độc tố [3].
Dù có nhiều tiến bộ trong lĩnh vực chăm sóc sản khoa, việc dự đoán và chẩn đoán sớm nguy cơ sinh non tự phát vẫn gặp phải nhiều rào cản lớn vì sinh non không phải là một bệnh lý đơn lẻ mà là một hội chứng phức tạp xuất phát từ nhiều nguyên nhân khác nhau (như nhiễm trùng, viêm nhiễm, yếu tố xã hội, di truyền) [9]. Các quy trình đánh giá rủi ro hiện tại thường chỉ phát huy hiệu quả ở giai đoạn muộn của thai kỳ, làm giảm cơ hội áp dụng các biện pháp can thiệp phòng ngừa. Hơn nữa, các phương pháp điều trị hiện tại (như sử dụng progesterone hay khâu cổ tử cung) được chứng minh là không giúp cải thiện hệ vi sinh âm đạo hay môi trường miễn dịch [9,15]. Sự đa dạng sinh học theo chủng tộc và địa lý dẫn đến sự khác biệt này khiến các chỉ số chẩn đoán (như độ đa dạng vi sinh) có thể đúng với quần thể này nhưng lại không áp dụng được cho quần thể khác [9,11]. Rào cản trong phân tích dữ liệu đa trung tâm gây cản trở lớn trong việc xác định các dấu ấn sinh học có thể nhân rộng và áp dụng phổ quát giữa các nghiên cứu khác nhau [9].
Để vượt qua những thách thức trên, lĩnh vực sản khoa đang hướng tới tầm nhìn y học cá thể hóa, kết hợp chặt chẽ giữa di truyền vật chủ, hệ vi sinh và công nghệ tính toán:
- Tích hợp di truyền vật chủ (nhóm máu ABO và gen FUT2) vào sàng lọc là một hướng đi đầy hứa hẹn, trong đó sử dụng xét nghiệm nhóm máu ABO (vốn đã được thực hiện thường quy đầu thai kỳ) kết hợp với thông tin về trạng thái tiết FUT2 để phân tầng nguy cơ sinh non. Nghiên cứu chỉ ra rằng phụ nữ nhóm máu O và B có nguy cơ sinh non cao hơn do hệ vi sinh âm đạo bất lợi (đa dạng cao, ít vi khuẩn có lợi) và môi trường dễ viêm nhiễm [9,15]. Ngược lại, phụ nữ nhóm máu A có xu hướng mang vi khuẩn bảo vệ Lactobacillus crispatus cao hơn và nguy cơ sinh non thấp hơn [15]. Đây là cánh cửa mở ra các can thiệp nhắm mục tiêu dựa trên sinh học thay vì các phương pháp chung chung.
- Sử dụng trí tuệ nhân tạo (AI) và học bởi máy (Machine Learning) trên dữ liệu "đa omics": y học cá thể hóa đang tận dụng sức mạnh của các mô hình học máy để phân tích bộ dữ liệu khổng lồ bao gồm hệ vi sinh, hệ chuyển hóa, hệ miễn dịch và hệ protein (multi-omics) cùng với dữ liệu lâm sàng. Các sáng kiến cộng đồng (như Microbiome PTB DREAM Challenge) đã phát triển thành công các thuật toán có khả năng dự đoán sinh non từ rất sớm (với độ chính xác AUROC lên tới 0,87 – 0,89) thông qua việc nhận diện các tín hiệu sinh học thay đổi theo thời gian trong quá trình mang thai [9].
- Liệu pháp can thiệp hệ vi sinh theo hướng cá thể hóa (Microbiota-directed therapies): dựa trên hồ sơ gen và vi sinh của từng bệnh nhân, các nhà khoa học đang thử nghiệm các phương pháp can thiệp chính xác hơn. Ví dụ, các thử nghiệm lâm sàng (như nghiên cứu PRIORI) đang đánh giá việc sử dụng các chế phẩm sinh học (probiotics như chủng Lactobacillus crispatus), synbiotics (kết hợp lợi khuẩn và thức ăn cho lợi khuẩn), hoặc thậm chí cấy ghép hệ vi sinh âm đạo (VMT) để phục hồi môi trường âm đạo cho nhóm phụ nữ nguy cơ cao [16]. Tương lai của y học cá thể hóa sẽ là xác định chính xác chủng vi khuẩn nào đang thiếu hụt và thiết kế phác đồ bổ sung phù hợp cho từng thai phụ, hoặc điều chỉnh dựa trên nhóm máu của họ [11].
Tóm lại, gen FUT2 đóng vai trò là một mắt xích không thể tách rời trong chuỗi cơ chế bảo vệ sức khỏe sinh sản. Bằng cách định hình bối cảnh glycan tại niêm mạc, FUT2 không chỉ lựa chọn hệ vi sinh vật cộng sinh mà còn thiết lập một hệ thống bảo vệ đa tầng trước các tác nhân nhiễm trùng. Sự hiểu biết sâu sắc về cầu nối giữa di truyền vật chủ và vi sinh học không chỉ giúp chúng ta giải mã được bí ẩn của sinh non mà còn đặt nền móng cho các chiến lược can thiệp sớm, mang tính cá thể hóa cao, nhằm đảm bảo một thai kỳ an toàn và khỏe mạnh cho mọi thai phụ.
1. Lipoldová M, Demant P. Gene-Specific Sex Effects on Susceptibility to Infectious Diseases. Front Immunol. 2021 Oct 14;12. doi:10.3389/fimmu.2021.712688
2. Chen J, Levintow S, Tran H, Sripaipan T, Nguyen M, Nguyen S, et al. HIV and STI prevalence and testing history among men who have sex with men in Hanoi, Vietnam. Int J STD AIDS. 2022 Feb;33(2):193–201. doi:10.1177/09564624211060185 PubMed PMID: 34852691; PubMed Central PMCID: PMC12219391.
3. Kaur P, Gupta M, Sagar V. FUT2 gene as a genetic susceptible marker of infectious diseases: A Review. Int J Mol Epidemiol Genet. 2022 Jun 15;13(1):1–14. PubMed PMID: 35892094; PubMed Central PMCID: PMC9301175.
4. Royse KE, Kempf MC, McGwin G, Wilson CM, Tang J, Shrestha S. Toll-Like Receptor Gene Variants Associated with Bacterial Vaginosis among HIV-1 Infected Adolescents. J Reprod Immunol. 2012 Dec;96(1–2):84–9. doi:10.1016/j.jri.2012.08.002 PubMed PMID: 23021866; PubMed Central PMCID: PMC3518650.
5. Routsias J, Verra C, Tsiakalos A, Tsakris A, Mavrouli M. The Role of TLR2/TLR4 Receptors in Host Genetic Susceptibility to Recurrent Vulvovaginitis. J Fungi. 2025 Nov 12;11(11):804. doi:10.3390/jof11110804 PubMed PMID: 41295183; PubMed Central PMCID: PMC12653547.
6. Lv X, Huang Z, Li S, Xu X, Chen D, Han L, et al. Correlation Of Fut2 And Fut3 Gene Polymorphisms With Inflammatory Bowel Disease In Guangxi Zhuang Population. Int J Gen Med. 2025 Mar 1;18:1217–30. doi:10.2147/IJGM.S505711 PubMed PMID: 40046452; PubMed Central PMCID: PMC11881759.
7. Nordgren J, Ågren R, Hu DZ, Neijd M, Childebayeva A, Prüfer K, et al. Natural Selection of a Virus-Protective FUT2 Variant Following the Transition to Agriculture. Mol Biol Evol. 2025 Oct 24;42(10):msaf243. doi:10.1093/molbev/msaf243 PubMed PMID: 41132048; PubMed Central PMCID: PMC12550361.
8. Kundu S, dos Santos Correia G, Lee YS, Ng S, Sykes L, Chan D, et al. Secretor status is a modifier of vaginal microbiota-associated preterm birth risk. Microb Genomics. 2024 Dec 4;10(12):001323. doi:10.1099/mgen.0.001323 PubMed PMID: 39630497; PubMed Central PMCID: PMC11616779.
9. Golob JL, Oskotsky TT, Tang AS, Roldan A, Chung V, Ha CWY, et al. Microbiome Preterm Birth DREAM Challenge: Crowdsourcing Machine Learning Approaches to Advance Preterm Birth Research. medRxiv. 2023 Apr 11;2023.03.07.23286920. doi:10.1101/2023.03.07.23286920 PubMed PMID: 36945505; PubMed Central PMCID: PMC10029035.
10. Nori SRC, Walsh CJ, McAuliffe FM, Moore RL, Van Sinderen D, Feehily C, et al. Strain-level variation among vaginal Lactobacillus crispatus and Lactobacillus iners as identified by comparative metagenomics. NPJ Biofilms Microbiomes. 2025 Mar 23;11:49. doi:10.1038/s41522-025-00682-1 PubMed PMID: 40122890; PubMed Central PMCID: PMC11930926.
11. Cheng D, Li N, Sun Q, Wang K, Gao F. Vaginal microbiome and preterm birth: Composition, mechanisms and microbiota-directed therapies (Review). Int J Mol Med. 2025 Sep 23;56(6):203. doi:10.3892/ijmm.2025.5644 PubMed PMID: 40999955; PubMed Central PMCID: PMC12488211.
12. Liang Y, Zhao C, Wen Y, Sheng D, Wei T, Hu T, et al. Modulation of local immunity by the vaginal microbiome is associated with triggering spontaneous preterm birth. Front Immunol. 2024 Nov 18;15:1481611. doi:10.3389/fimmu.2024.1481611 PubMed PMID: 39624094; PubMed Central PMCID: PMC11609181.
13. Talbert JA, Spicer SK, Manning SD, Gaddy JA, Townsend SD. Human Milk Oligosaccharides Mediate the Host–Microbe Interface in a Model Vaginal Community. ACS Infect Dis. 11(6):1729–40. doi:10.1021/acsinfecdis.5c00295 PubMed PMID: 40459557; PubMed Central PMCID: PMC12172043.
14. Jimenez NR, Maarsingh JD. Commensal Lactobacilli Metabolically Contribute to Cervical Epithelial Homeostasis in a Species-Specific Manner. mSphere. 8(1):e00452-22. doi:10.1128/msphere.00452-22 PubMed PMID: 36629413; PubMed Central PMCID: PMC9942568.
15. Mountain KE, MacIntyre DA, Lee YS, Tajadura-Ortega V, Dell A, Haslam SM, et al. ABO blood group antigens influence host–microbe interactions and risk of early spontaneous preterm birth. NPJ Biofilms Microbiomes. 2025 Sep 10;11:170. doi:10.1038/s41522-025-00783-x PubMed PMID: 40931094; PubMed Central PMCID: PMC12423329.
16. Nulens K, Papy E, Tartaglia K, Dehaene I, Logghe H, Van Keirsbilck J, et al. Synbiotics in patients at risk for spontaneous preterm birth: protocol for a multi-centre, double-blind, randomised placebo-controlled trial (PRIORI). Trials. 2024 Sep 17;25:615. doi:10.1186/s13063-024-08444-8 PubMed PMID: 39289685; PubMed Central PMCID: PMC11406859.