1. Giới thiệu
Trưởng thành noãn là một quá trình sinh học phức tạp, bao gồm sự phối hợp chặt chẽ giữa trưởng thành nhân và trưởng thành bào tương, dưới sự điều hòa của các cơ chế phân tử, nội tiết và tương tác giữa noãn với tế bào hạt. Quá trình này đóng vai trò quyết định đối với khả năng thụ tinh và sự phát triển phôi. Tuy nhiên, trong một số trường hợp, noãn không thể hoàn tất quá trình trưởng thành và bị ngừng ở các giai đoạn khác nhau của giảm phân, gây thất bại thụ tinh hoặc vô sinh, tình trạng này được gọi là ngừng trưởng thành noãn (oocyte maturation arrest – OMA). Mặc dù hiếm gặp, OMA có ý nghĩa lâm sàng quan trọng do liên quan đến thất bại điều trị lặp lại và chi phí cao [1]. Các bằng chứng gần đây cho thấy OMA là một phổ rối loạn không đồng nhất, liên quan đến nhiều cơ chế như đột biến gen, rối loạn tín hiệu nội bào, bất thường biểu sinh và thay đổi môi trường vi nang. Do đó, bài tổng quan này nhằm tổng hợp các cơ chế sinh học liên quan đến sự trưởng thành của noãn, phân tích các nguyên nhân gây ngừng trưởng thành noãn và thảo luận các chiến lược điều trị hiện nay trong thực hành hỗ trợ sinh sản.
2. Cơ chế trưởng thành noãn
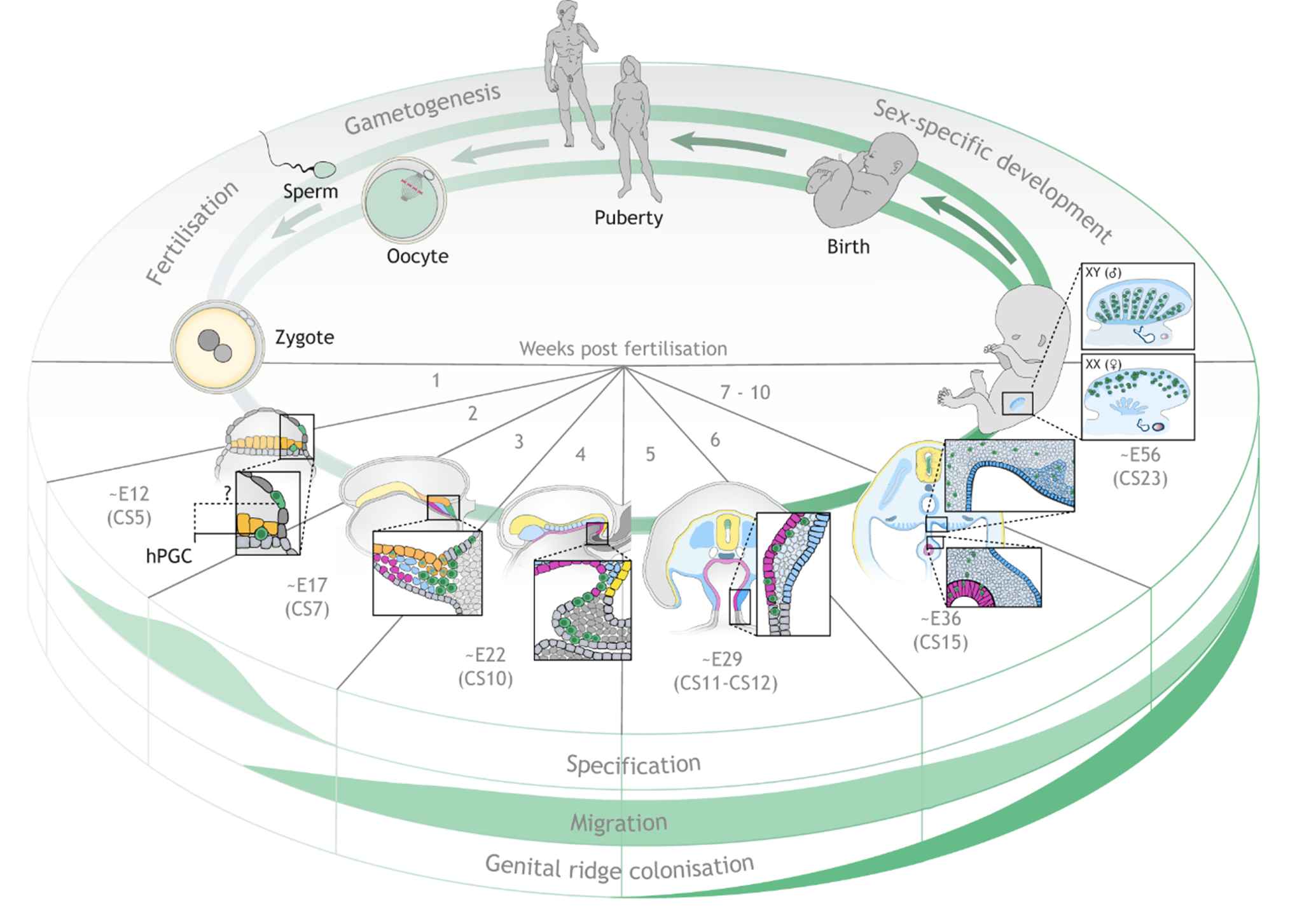
Noãn bắt đầu giảm phân từ thời kỳ bào thai và bị ngừng ở giai đoạn diplotene của kỳ đầu I cho đến tuổi dậy thì. Sự ngừng này được duy trì nhờ nồng độ cAMP cao trong noãn, kết quả của sự phối hợp chặt chẽ giữa noãn và các tế bào hạt xung quanh.
Noãn tự sản sinh cAMP thông qua hệ thống GPR3 – protein Gs – adenylyl cyclase (AC3). GPR3 hoạt động liên tục trên màng noãn, kích hoạt Gs và AC3 để tạo cAMP. Nồng độ cAMP cao hoạt hóa PKA, từ đó ức chế CDK1 và giữ yếu tố thúc đẩy trưởng thành (Maturation-Promoting Factor - MPF) ở trạng thái bất hoạt, giúp duy trì ngừng giảm phân. Nếu cAMP giảm (ví dụ khi noãn bị tách khỏi nang), quá trình giảm phân sẽ tự phát tiếp tục.
Tuy nhiên, cAMP nội sinh từ noãn là chưa đủ. Tế bào hạt đóng vai trò quan trọng thông qua hệ thống NPPC/NPR2. NPPC do tế bào hạt tiết ra gắn vào thụ thể NPR2 trên tế bào hạt cumulus, kích thích sản sinh cGMP. cGMP được vận chuyển vào noãn và ức chế PDE3A, enzyme phân hủy cAMP. Nhờ đó, cAMP trong noãn được duy trì ở mức cao, đảm bảo tình trạng ngừng GV kéo dài.
Sự tái khởi động giảm phân xảy ra khi có đỉnh LH trước rụng trứng. LH làm giảm biểu hiện và hoạt tính của hệ thống NPPC/NPR2, dẫn đến giảm cGMP trong tế bào hạt và noãn. Khi cGMP giảm, PDE3A được giải phóng khỏi ức chế, phân hủy cAMP. Sự sụt giảm cAMP cho phép hoạt hóa MPF, gây vỡ túi mầm (Germinal Vesicle Breakdown - GVBD) và tái khởi động giảm phân [2].
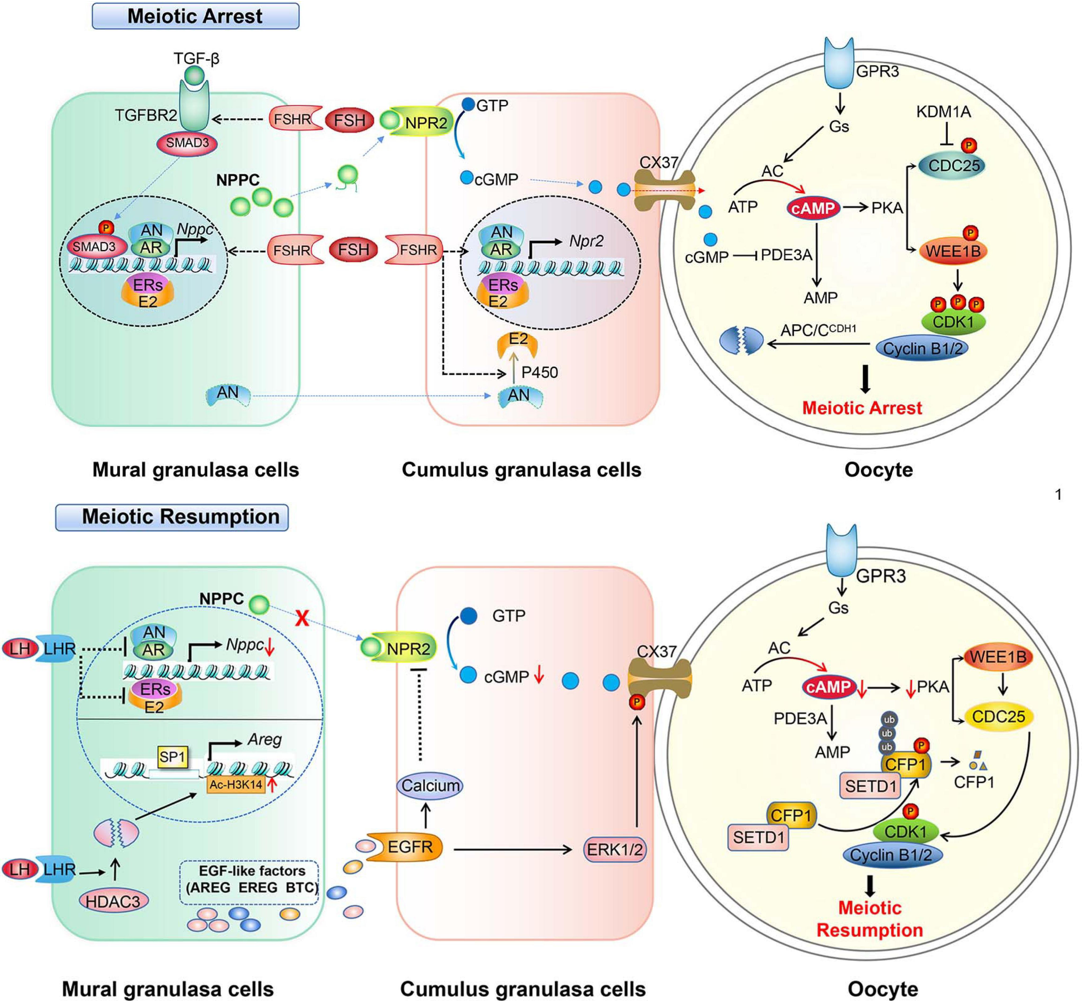
Hình 1. Cơ chế điều hòa ngừng và tiếp tục giảm phân của noãn [2]
Sự tiếp tục giảm phân của noãn được khởi phát bởi đỉnh LH trước rụng trứng thông qua cơ chế điều hòa phối hợp giữa tế bào hạt và noãn bào. LH gắn vào thụ thể LHR trên tế bào hạt, gây giảm hoạt động của hệ thống NPPC/NPR2, từ đó làm giảm sản sinh cGMP và đóng các khe nối giữa tế bào hạt và noãn. Khi cGMP giảm, PDE3A trong noãn được giải phóng khỏi ức chế, dẫn đến phân hủy cAMP nội bào. Sự sụt giảm cAMP làm giảm hoạt tính PKA, cho phép phosphatase CDC25 hoạt hóa CDK1 bằng cách khử phosphoryl hóa các vị trí ức chế, trong khi WEE1 bị bất hoạt. CDK1 kết hợp với cyclin B hình thành MPF, yếu tố trung tâm điều khiển sự tái khởi động giảm phân. MPF hoạt hóa gây vỡ túi mầm (GVBD), thúc đẩy ngưng tụ nhiễm sắc thể, hình thành thoi phân bào và khởi động phân tách nhiễm sắc thể.
Sự tổng hợp và tích lũy cyclin B1 là điều kiện tiên quyết cho hoạt hóa MPF, trong khi phức hợp APC/C–CDH1 liên tục phân hủy cyclin B để duy trì trạng thái ngừng trước đó. Ngoài ra, LH còn kích thích mạng lưới các yếu tố tăng trưởng giống biểu bì (EGF) trong tế bào hạt, hoạt hóa EGFR và các tín hiệu MAPK, đồng thời kích hoạt PDE5 và làm đóng các khe nối connexin (Cx43, Cx37), từ đó khuếch đại sự giảm cGMP và cAMP trong noãn. Các cơ chế biểu sinh như điều hòa HDAC3 trong tế bào hạt cũng góp phần kiểm soát biểu hiện AREG và đáp ứng với LH. Tín hiệu Ca²⁺ nội bào trong tế bào hạt tiếp tục bất hoạt NPR2, củng cố quá trình giảm cGMP. Như vậy, sự tiếp tục giảm phân của noãn là kết quả của việc LH phá vỡ trục duy trì cGMP–cAMP, giải phóng hoạt hóa MPF và đồng thời huy động các tín hiệu EGF, MAPK và Ca²⁺ để đảm bảo noãn trưởng thành và sẵn sàng rụng trứng [2].
3. Sự ngừng phát triển của noãn
3.1. Khái niệm
Sự ngừng trưởng thành noãn (Oocyte Maturation Arrest – OMA) là tình trạng noãn không thể hoàn tất quá trình trưởng thành giảm phân, dẫn đến sự xuất hiện chủ yếu các noãn chưa trưởng thành trong chu kỳ IVF/ICSI và gây thất bại thụ tinh hoặc vô sinh [1].
Khi tỷ lệ noãn chưa trưởng thành vượt quá 25%, tỷ lệ thụ tinh, tỷ lệ tạo phôi nang và tỷ lệ thai lâm sàng giảm đáng kể, khi vượt quá 40%, quá trình trưởng thành nhân của noãn có thể bị bất thường và việc đạt được thai kỳ lâm sàng trở nên rất khó khăn [3].
Tuy nhiên, cần phân biệt giữa hiện tượng OMA “thỉnh thoảng” với hội chứng thất bại trưởng thành noãn lặp lại (syndrome of repeated oocyte maturation failure - ROMF). ROMF là hội chứng lâm sàng của OMA lặp lại, trong đó phần lớn noãn thu được qua nhiều chu kỳ IVF/ICSI đều ở trạng thái chưa trưởng thành. Ở một số trường hợp nặng, tình trạng này có thể biểu hiện hoàn toàn, tức không thu được noãn trưởng thành nào. Các bệnh nhân này thường có một số đặc điểm chung như (1) vô sinh nguyên phát; (2) lặp đi lặp lại sự tạo thành chủ yếu các noãn chưa trưởng thành; (3) không thể kích thích trưởng thành noãn bằng nuôi trưởng thành trong ống nghiệm (IVM); và (4) thất bại thụ tinh ngay cả khi thực hiện tiêm tinh trùng vào bào tương noãn (ICSI) [4].
Trong khi đó, hiện tượng OMA “thỉnh thoảng” dùng để chỉ hiện tượng đôi khi thu nhận được noãn chưa trưởng thành, thường do các yếu tố kỹ thuật hoặc môi trường nuôi cấy in vitro, chẳng hạn như phương pháp trigger không phù hợp hoặc thời điểm chọc hút noãn chưa tối ưu [3].
3.2. Phân loại OMA
Việc phân loại OMA có ý nghĩa quan trọng trong chẩn đoán, tiên lượng và định hướng điều trị [3], [5]. Tuy nhiên, cho đến nay vẫn chưa có hệ thống phân loại thống nhất. Trước đây, Beall và cộng sự (2010) gọi hiện tượng thất bại trưởng thành noãn là “bad egg syndrome” và chủ yếu được phân loại dựa trên đặc điểm hình thái của noãn, tương quan với các giai đoạn của quá trình giảm phân, bao gồm bốn nhóm: loại I-ngừng ở giai đoạn GV, loại II-ngừng ở giai đoạn MI, loại III-ngừng ở giai đoạn MII và loại IV-ngừng hỗn hợp GV, MI và MII [4].
Sau đó, Hatirnaz-Dahan và cộng sự (2019) đã đề xuất hệ thống phân loại ở mức độ bệnh nhân, với loại I ngừng GV, loại II ngừng MI, loại III ngừng MII, loại IV ngừng kết hợp GV–MI và ngừng hỗn hợp ở nhiều giai đoạn (GV, MI và MII) được xếp vào loại V, hệ thống này chỉ áp dụng khi toàn bộ noãn đều chưa trưởng thành[6].
Tuy nhiên, trong thực hành lâm sàng, bệnh nhân thường thu được cả noãn trưởng thành và chưa trưởng thành, ngay cả sau khi điều chỉnh phác đồ kích thích buồng trứng. Do đó, Lixia Zhu và cộng sự (2022) đề xuất hệ thống phân loại dựa trên giai đoạn ngưng trệ chiếm ưu thế (>50%) trong đoàn hệ noãn, gồm 3 nhóm: loại I khi >50% noãn dừng ở giai đoạn GV; loại II >50% noãn dừng ở kỳ giữa I (MI); và loại III (ngừng hỗn hợp) khi không có giai đoạn đơn lẻ nào vượt 50% nhưng tổng số noãn chưa trưởng thành (GV + MI) chiếm >50% [3].
4. Cơ chế bệnh sinh
Cơ chế bệnh sinh của OMA là một quá trình phức tạp và vẫn chưa được hiểu đầy đủ,
liên quan đến sự gián đoạn của quá trình giảm phân bình thường do các đột biến di truyền, rối loạn tín hiệu phân tử, khiếm khuyết ty thể và các yếu tố môi trường vi mô nang noãn.
4.1. Đột biến gen
Trong những năm gần đây, sự ứng dụng của giải trình tự toàn bộ vùng mã hóa (Whole Exome Sequencing – WES) đã giúp xác định nhiều gen liên quan trực tiếp đến quá trình giảm phân và trưởng thành noãn, qua đó củng cố giả thuyết rằng OMA có nền tảng di truyền quan trọng [3].
a. Nhóm rối loạn hình thành thoi phân bào
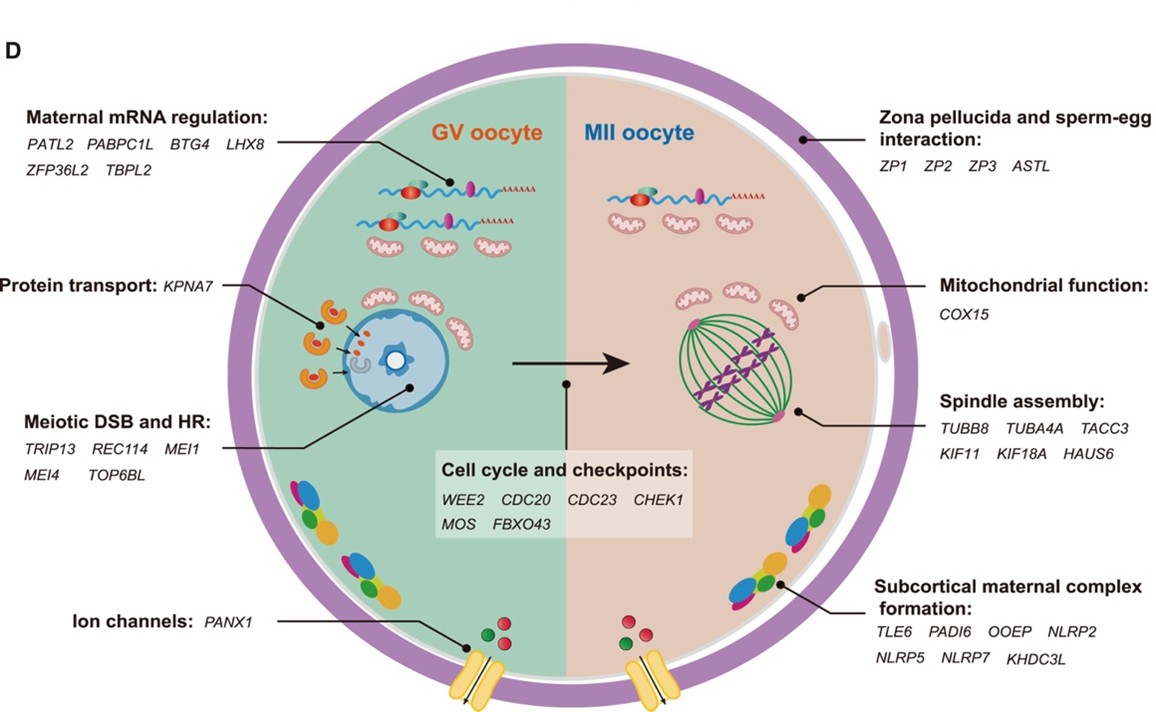
TUBB8 (tubulin beta 8 class VIII) là gen được báo cáo thường gặp nhất trong cơ chế di truyền của OMA, với khoảng 30% bệnh nhân được ghi nhận mang biến thể này [7], [8]. TUBB8 nằm trên nhiễm sắc thể 10p15.3, gồm bốn exon và mã hóa một protein dài 444 axit amin. TUBB8 là gen mã hóa β-tubulin đặc hiệu ở noãn người, giữ vai trò thiết yếu trong sự hình thành và ổn định của thoi phân bào giảm phân. Đột biến TUBB8 làm rối loạn cấu trúc vi ống, gây bất thường trong sắp xếp và phân ly nhiễm sắc thể, từ đó dẫn đến ngừng trưởng thành noãn, thường gặp nhất ở giai đoạn MI. Ngoài TUBB8, các biến thể trong năm gen liên quan đến lắp ráp thoi phân bào khác- TUBA4A , KIF11 , HAUS6 , TACC3 và KIF18A [9].
b. Nhóm rối loạn điểm kiểm soát chu kỳ tế bào và điều hòa chu kỳ tế bào trong giảm phân
Nhóm này bao gồm các gen tham gia kiểm soát tiến trình giảm phân, đặc biệt là sự chuyển tiếp từ kỳ giữa sang kỳ sau.
TRIP13 là một thành phần quan trọng của điểm kiểm soát lắp ráp thoi vô sắc (spindle assembly checkpoint – SAC). Đột biến TRIP13 có thể gây hoạt hóa checkpoint kéo dài, khiến noãn không thể vượt qua kỳ giữa I và dẫn đến ngừng MI. Một số nghiên cứu thực nghiệm cho thấy việc bổ sung RNA mã hóa TRIP13 có thể phục hồi một phần chức năng, gợi ý tiềm năng ứng dụng điều trị trong tương lai [7], [8].
CDC20 là đồng hoạt hóa của phức hợp APC/C, có vai trò thúc đẩy phân hủy securin và cyclin B để noãn chuyển từ metaphase sang anaphase. Khi CDC20 bị đột biến, noãn không thể hoàn tất quá trình phân tách nhiễm sắc thể tương đồng, dẫn đến rối loạn trưởng thành noãn và phát triển phôi sớm. Do đó, CDC20 được xem là một gen quan trọng trong nhóm rối loạn điểm kiểm soát chu kỳ tế bào của OMA [7], [8].
WEE2 (WEE1 homolog 2) nằm trên nhiễm sắc thể 7q34, gồm 12 exon và mã hóa một protein dài 567 axit amin. WEE2, còn gọi là Wee1B, là một kinase tyrosine đặc hiệu của noãn, thuộc họ WEE kinase và đóng vai trò quan trọng điều hòa hoạt động của CDK1 và phức hợp MPF. Ở giai đoạn GV, WEE2 duy trì tình trạng ngừng giảm phân bằng cách ức chế MPF thông qua bất hoạt CDK1. Sau thụ tinh, WEE2 tham gia điều hòa quá trình thoát khỏi trạng thái ngừng ở metaphase II. Các đột biến ở WEE2 có thể làm MPF duy trì hoạt tính cao bất thường, khiến noãn không thể thoát khỏi MII sau thụ tinh và dẫn đến thất bại thụ tinh [8].
c. Nhóm rối loạn điều hòa mRNA của mẹ
Sự trưởng thành của noãn phụ thuộc chặt chẽ vào việc dự trữ, ổn định và phân hủy đúng thời điểm các mRNA có nguồn gốc từ mẹ. Rối loạn ở nhóm gen này có thể làm gián đoạn dịch mã và các sự kiện chuẩn bị cho giảm phân.
PATL2 là một yếu tố điều hòa dịch mã đặc hiệu của noãn, được biểu hiện mạnh ở noãn chưa trưởng thành và giảm dần khi noãn tiến tới giai đoạn trưởng thành. Các biến thể gây bệnh của PATL2 đã được ghi nhận ở bệnh nhân vô sinh do ngừng GV hoặc ngừng MI, thường kèm theo thất bại thụ tinh và ngừng phát triển phôi sớm. Các dữ liệu chức năng cho thấy PATL2 có vai trò quan trọng trong điều hòa dịch mã mRNA mẹ và bảo đảm tiến trình giảm phân bình thường [8].
PABPC1L mã hóa một protein liên kết với đuôi poly(A) của mRNA, tham gia ổn định mRNA và kích hoạt dịch mã các mRNA của mẹ cần thiết cho trưởng thành noãn. Đột biến hai alen của PABPC1L có thể gây hoạt hóa quá mức trục Mos–MAPK, duy trì trạng thái ngưng trệ giảm phân và dẫn đến ngừng MII [10].
ZFP36L2 là một protein liên kết RNA có vai trò quan trọng trong điều hòa sự phân hủy mRNA của mẹ. Biến thể gây bệnh ở ZFP36L2 có thể làm giảm tính ổn định của mRNA và suy giảm chức năng phân hủy mRNA mẹ, từ đó ảnh hưởng đến trưởng thành noãn. Những dữ liệu này cho thấy ZFP36L2 là một gen ứng viên tiềm năng trong chẩn đoán di truyền các rối loạn trưởng thành noãn [10].
TBPL2 là một yếu tố phiên mã chung đặc hiệu của noãn ở động vật có xương sống, có vai trò trong khởi đầu phiên mã của nhiều gen cần thiết cho trưởng thành noãn và khả năng thụ tinh. Đột biến TBPL2 làm suy giảm biểu hiện của các gen liên quan đến trưởng thành noãn, gây rối loạn điều hòa transcriptome của noãn và dẫn đến ngưng trệ trưởng thành hoặc thoái hóa noãn. Vì vậy, TBPL2 đại diện cho nhóm gen điều hòa phiên mã có vai trò quan trọng trong bệnh sinh của OMA [7].
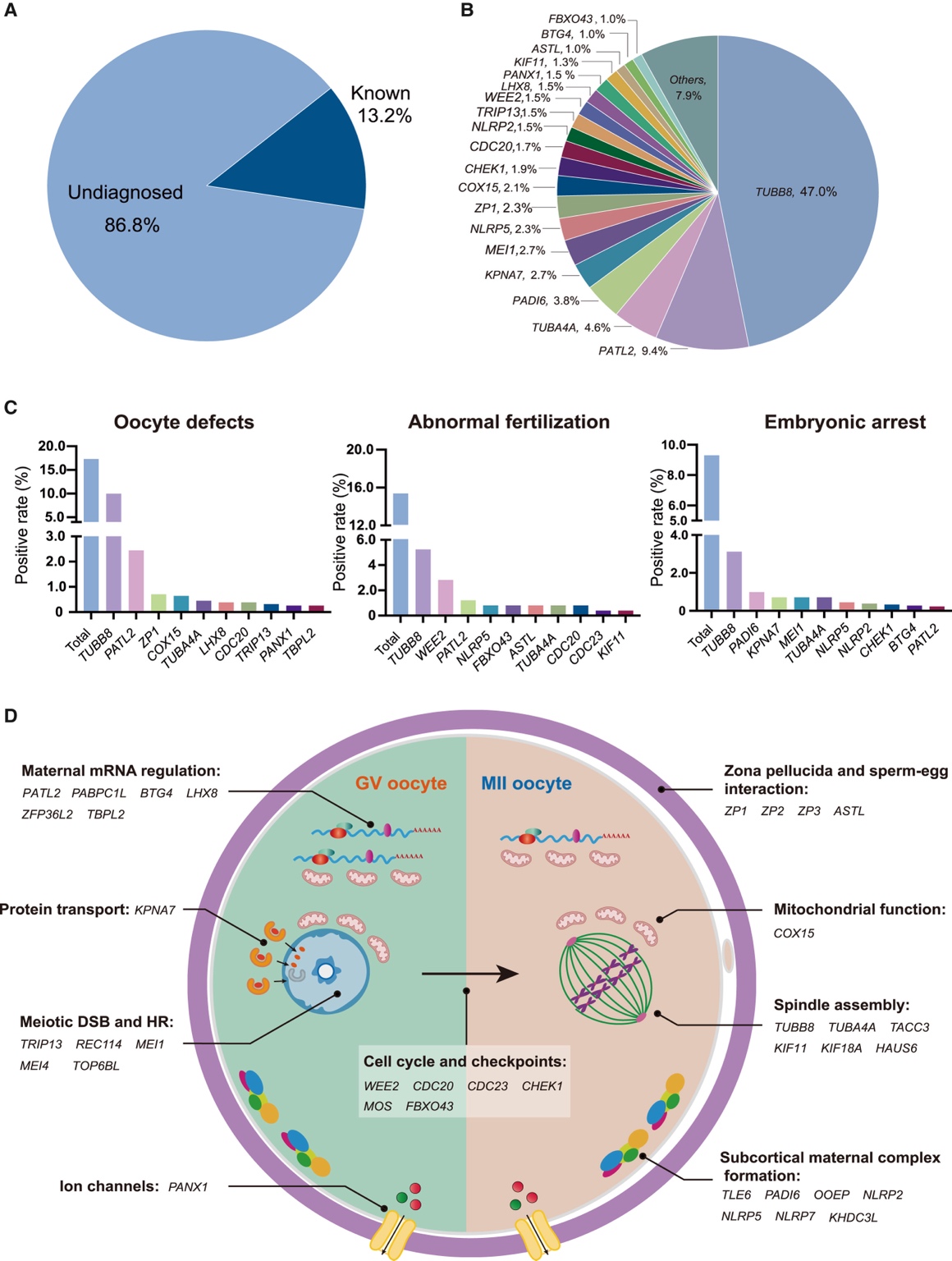
Hình 2. Tổng quan về nhóm bệnh nhân được xác định có gen gây bệnh đã biết liên quan đến các khiếm khuyết ở noãn bào/phôi [9].
4.2. Rối loạn con đường tín hiệu
a. Rối loạn trục PDE3–Cdc25–CDK1
Ở người, noãn bị ngừng ở kỳ đầu giảm phân I (GV) cho đến khi dậy thì. Trong chu kỳ kinh nguyệt, sự gia tăng hormone luteinizing (LH) kích hoạt con đường tín hiệu cAMP–Cdc25, làm tăng hoạt động của PDE3, dẫn đến thủy phân cAMP và hoạt hóa MPF- một phức hợp gồm CDK1 và cyclin B. Sự hoạt hóa MPF thúc đẩy phân hủy túi mầm (GVBD) và cho phép noãn tiếp tục tiến trình giảm phân. Do đó, đột biến hoặc mất chức năng của các thành phần trong trục PDE3–Cdc25–CDK1 có thể ngăn cản hoạt hóa MPF, khiến noãn không thể tái khởi động giảm phân và bị ngừng ở giai đoạn GV.
b. Lỗi tại các điểm kiểm soát (SAC và APC/C)
Sự tiến triển qua giảm phân I đòi hỏi sự hình thành thoi phân bào chính xác và bất hoạt kịp thời điểm kiểm soát lắp ráp thoi phân bào (spindle assembly checkpoint -SAC), hoạt hóa SAC kéo dài hoặc rối loạn phức hợp APC/C sẽ cản trở phân hủy securin và cyclin B, gây ngừng ở kỳ giữa I (ngừng MI).
c. Yếu tố thúc đẩy trưởng thành (MPF)
Ngừng sinh lý ở kỳ giữa II (ngừng MII) được duy trì bởi MPF cao dưới sự điều hòa của CSF và con đường Mos/MAPK. Sau thụ tinh, các dao động Ca²⁺ nội bào kích hoạt CaMKII và APC/C, thúc đẩy sự phân hủy cyclin B và giúp noãn thoát khỏi MII để hoàn tất giảm phân. Sự rối loạn của các cơ chế điều hòa này có thể khiến noãn không hoàn thành giảm phân II (ngừng MII) [4], [3], [6], [10].
Nhìn chung, OMA không phải là một thực thể đơn nhất mà là một phổ rối loạn phức tạp, trong đó sự gián đoạn tại các điểm điều hòa khác nhau của quá trình giảm phân có thể dẫn đến các kiểu hình ngừng phát triển khác nhau. Việc hiểu rõ cơ chế phân tử của từng loại OMA có ý nghĩa quan trọng trong chẩn đoán, tiên lượng và xây dựng chiến lược điều trị cá thể hóa [5].
4.3. Tác động bệnh lý và môi trường
Một số yếu tố ngoài di truyền có thể ảnh hưởng gián tiếp đến quá trình trưởng thành noãn thông qua thay đổi môi trường nội nang:
a. Lạc nội mạc tử cung: Dịch nang trứng ở bệnh nhân lạc nội mạc tử cung thường chứa nồng độ cao các gốc oxy hóa phản ứng (ROS), có thể gây tổn thương DNA của noãn. Tổn thương này kích hoạt phản ứng tổn thương DNA (DDR) và con đường điểm kiểm soát thoi vô sắc (SAC), dẫn đến sự ngừng tiến triển giảm phân ở giai đoạn kỳ giữa I (MI) [10].
b. Hội chứng buồng trứng đa nang (PCOS): PCOS gây ra các rối loạn nội tiết và chuyển hóa phức tạp, có thể ảnh hưởng đến quá trình trưởng thành của noãn. Ở bệnh nhân PCOS, sự giảm biểu hiện của protein sốc nhiệt Hsp27 trong mô buồng trứng được ghi nhận có liên quan đến sự suy giảm trưởng thành của noãn. Ngoài ra, biểu hiện bất thường của endothelin-1 (ET-1) trong tế bào hạt, cùng với sự hoạt hóa quá mức của trục NPPC/NPR2, có thể làm tăng tích lũy cAMP, từ đó cản trở quá trình tái khởi động giảm phân[11]. Bên cạnh đó, các thay đổi biểu sinh như giảm biểu hiện miR-514 và miR-642b trong tế bào cumulus bao quanh noãn cũng được xem là dấu hiệu liên quan đến chất lượng noãn kém ở bệnh nhân PCOS [10].
c. Tuổi mẹ cao: Lão hóa là yếu tố quan trọng làm gia tăng sai sót trong quá trình phân ly nhiễm sắc thể, dẫn đến tỷ lệ noãn lệch bội cao. Đồng thời, sự suy giảm chức năng ty thể và sự tích tụ các đột biến DNA ty thể (mtDNA), điển hình như mất đoạn 4,9 kb, có thể làm giảm sản xuất ATP. Sự thiếu hụt năng lượng này ảnh hưởng đến sự hình thành thoi vô sắc và sự phân tách nhiễm sắc thể, từ đó làm tăng nguy cơ ngừng phát triển của noãn hoặc phôi [12].
d. Độc chất môi trường: Tiếp xúc với Bisphenol A (BPA) ở nồng độ cao có thể gây rối loạn cấu trúc thoi vô sắc và sự sắp xếp nhiễm sắc thể trên đĩa xích đạo, dẫn đến sự ngừng tiến triển giảm phân ở giai đoạn kỳ giữa I (MI) [5]. Do đó, cần giảm phơi nhiễm BPA trong môi trường sống và tiêu dùng, đồng thời tăng cường kiểm soát chất lượng phòng thí nghiệm bằng cách ưu tiên sử dụng vật liệu tiêu hao không chứa BPA hoặc đã được chứng nhận an toàn cho noãn và phôi.
5. Hướng điều trị
Việc điều trị hội chứng ngừng trưởng thành noãn vẫn còn nhiều thách thức do cơ chế bệnh sinh phức tạp và thường liên quan đến các khiếm khuyết nội tại của noãn.
5.1. Điều chỉnh phác đồ kích thích buồng trứng
Trong trường hợp OMA “thỉnh thoảng”, việc điều chỉnh phác đồ kích thích buồng trứng có thể cải thiện kết quả lâm sàng. Các phương pháp đã được đề xuất bao gồm thay đổi phương thức và thời điểm kích thích, chẳng hạn như sử dụng dual trigger (kết hợp GnRH agonist và hCG), trì hoãn thời điểm trigger, hoặc kéo dài khoảng thời gian từ lúc trigger đến khi chọc hút noãn. Những điều chỉnh này có thể giúp tăng số lượng noãn đạt giai đoạn MII. Tuy nhiên, ở những bệnh nhân có OMA lặp lại, các chiến lược này thường không thể khắc phục được các khiếm khuyết trưởng thành nội tại của noãn [3], [13].
5.2. Nuôi trưởng thành noãn trong ống nghiệm (IVM)
Nuôi trưởng thành noãn trong ống nghiệm (IVM) có thể được sử dụng như một phương pháp cứu vãn ở những trường hợp thu được nhiều noãn chưa trưởng thành. Trong nghiên cứu của Lixia Zhu và cộng sự (2022), bệnh nhân được phân loại thành ba nhóm OMA (loại I ngừng GV, loại II ngừng MI và loại III ngừng hỗn hợp GV và MI) [3]. Kết quả cho thấy tỷ lệ trưởng thành sau IVM và tiềm năng phát triển phôi ở các nhóm OMA đều thấp hơn đáng kể so với nhóm đối chứng, đặc biệt ở nhóm ngừng MI.
Tương tự, trong nghiên cứu hồi cứu của Hatirnaz và cộng sự (2021) trên 63 bệnh nhân OMA lặp lại được điều trị bằng IVM có kích thích trước bằng FSH–hCG. Nghiên cứu này phân loại theo hệ thống Hatirnaz và Dahan gồm 5 loại OMA (trong đó loại I ngừng GV, loại II ngừng MI, loại III ngừng MII, loại 4 ngừng GV, MI và loại 5 ngừng hỗn hợp GV, MI và MII). Kết quả là số lượng noãn thu được thấp hơn so với chu kỳ IVF thông thường và không có phôi nào được tạo ra ở các nhóm OMA loại I, II và IV. Ở nhóm loại V, mặc dù có tạo được một số phôi ngày 2 và ngày 3, nhưng không ghi nhận trường hợp mang thai lâm sàng. Kết quả này cho thấy IVM có kích thích FSH–hCG không cải thiện đáng kể khả năng trưởng thành noãn hay kết cục lâm sàng ở bệnh nhân OMA lặp lại [14]. Ngược lại, IVM có thể hiệu quả ở các tình trạng như hội chứng nang trống, nơi khiếm khuyết chủ yếu liên quan đến tín hiệu nội tiết hoặc thụ thể hormone, thay vì các bất thường nội tại của noãn [5]. Như vậy, IVM kém hiệu quả trong OMA lặp lại do lỗi nội tại của noãn.
5.3. Xét nghiệm chẩn đoán di truyền
Giải trình tự toàn bộ vùng mã hóa (whole-exome sequencing – WES) đóng vai trò quan trọng trong việc xác định căn nguyên di truyền của OMA. Các đột biến ở các gen như TUBB8, PATL2, ZFP36L2 hoặc WEE2 đã được chứng minh có liên quan đến các kiểu hình ngừng trưởng thành noãn khác nhau. Do đó, xét nghiệm di truyền được khuyến nghị cho những bệnh nhân đã trải qua 2–3 chu kỳ IVF/ICSI thất bại do OMA và có kết quả IVM không đạt yêu cầu [3], [10].
5.4. Xin noãn
Trong các trường hợp OMA lặp lại hoặc liên quan đến các đột biến di truyền, xin noãn hiện được xem là lựa chọn điều trị hiệu quả nhất. Phương pháp này đặc biệt phù hợp với bệnh nhân mang các đột biến ở các gen liên quan đến trưởng thành noãn, khi khả năng sử dụng noãn tự thân rất thấp. Việc tư vấn xin noãn sớm có thể giúp giảm gánh nặng tâm lý, chi phí điều trị và tăng cơ hội đạt được thai kỳ thành công [3], [6].
6. Kết luận
Ngừng trưởng thành noãn là một rối loạn hiếm nhưng có ý nghĩa quan trọng trong hỗ trợ sinh sản, phản ánh sự rối loạn phức tạp của các cơ chế điều hòa trưởng thành noãn, bao gồm các con đường tín hiệu nội bào, tương tác noãn–tế bào hạt và các yếu tố di truyền, biểu sinh. Việc phân loại OMA theo kiểu hình ngừng trưởng thành giúp định hướng tiên lượng và lựa chọn chiến lược điều trị phù hợp.
Trong thực hành lâm sàng, các biện pháp như điều chỉnh phác đồ kích thích buồng trứng, kéo dài thời gian trigger–chọc hút hoặc nuôi trưởng thành noãn trong ống nghiệm có thể cải thiện kết quả ở một số trường hợp OMA “thỉnh thoảng”, nhưng hiệu quả còn hạn chế ở OMA lặp lại do liên quan đến các khiếm khuyết nội tại của noãn. Do đó, phân tích di truyền đóng vai trò quan trọng trong cá thể hóa điều trị. Trong các trường hợp tiên lượng xấu hoặc có đột biến gây bệnh, xin noãn hiện vẫn là lựa chọn hiệu quả nhất. Trong tương lai, việc hiểu rõ hơn các cơ chế phân tử của OMA có thể mở ra các chiến lược điều trị mới nhằm cải thiện kết quả sinh sản cho nhóm bệnh nhân này.
Tài liệu tham khảo
[1] W. Wang, Q. Sang, and L. Wang, ‘Genetic factors of oocyte maturation arrest: an important cause for recurrent IVF/ICSI failures’, J. Assist. Reprod. Genet., vol. 41, no. 8, pp. 1951–1953, Aug. 2024, doi: 10.1007/s10815-024-03195-6.
[2] M. He, T. Zhang, Y. Yang, and C. Wang, ‘Mechanisms of Oocyte Maturation and Related Epigenetic Regulation’, Front. Cell Dev. Biol., vol. 9, p. 654028, Mar. 2021, doi: 10.3389/fcell.2021.654028.
[3] L. Zhu et al., ‘Oocyte phenotype, genetic diagnosis, and clinical outcome in case of patients with oocyte maturation arrest’, Front. Endocrinol., vol. 13, Nov. 2022, doi: 10.3389/fendo.2022.1016563.
[4] S. Beall, C. Brenner, and J. Segars, ‘Oocyte maturation failure: a syndrome of bad eggs’, Fertil. Steril., vol. 94, no. 7, pp. 2507–2513, Dec. 2010, doi: 10.1016/j.fertnstert.2010.02.037.
[5] S. Hatirnaz et al., ‘Unraveling the Puzzle: Oocyte Maturation Abnormalities (OMAS)’, Diagnostics, vol. 12, no. 10, p. 2501, Oct. 2022, doi: 10.3390/diagnostics12102501.
[6] Ş. Hatırnaz et al., ‘Oocyte maturation abnormalities - A systematic review of the evidence and mechanisms in a rare but difficult to manage fertility pheneomina’, Turk. J. Obstet. Gynecol., vol. 19, no. 1, pp. 60–80, Mar. 2022, doi: 10.4274/tjod.galenos.2022.76329.
[7] A. Abbara, S. A. Clarke, and W. S. Dhillo, ‘Novel Concepts for Inducing Final Oocyte Maturation in In Vitro Fertilization Treatment’, Endocr. Rev., vol. 39, no. 5, pp. 593–628, Oct. 2018, doi: 10.1210/er.2017-00236.
[8] X. Ding and J. C. Schimenti, ‘Female infertility from oocyte maturation arrest: assembling the genetic puzzle’, EMBO Mol. Med., vol. 15, no. 6, p. EMMM202317729, Apr. 2023, doi: 10.15252/emmm.202317729.
[9] B. Chen et al., ‘Genetic landscape of human oocyte/embryo defects’, Cell Genomics, vol. 6, no. 1, p. 101012, Jan. 2026, doi: 10.1016/j.xgen.2025.101012.
[10] G. M. Baldini et al., ‘Genetic Abnormalities of Oocyte Maturation: Mechanisms and Clinical Implications’, Int. J. Mol. Sci., vol. 25, no. 23, Dec. 2024, doi: 10.3390/ijms252313002.
[11] Z. Pei, K. Deng, C. Xu, and S. Zhang, ‘The molecular regulatory mechanisms of meiotic arrest and resumption in Oocyte development and maturation’, Reprod. Biol. Endocrinol., vol. 21, no. 1, p. 90, Oct. 2023, doi: 10.1186/s12958-023-01143-0.
[12] O. A. Solovova and V. B. Chernykh, ‘Genetics of Oocyte Maturation Defects and Early Embryo Development Arrest’, Genes, vol. 13, no. 11, p. 1920, Oct. 2022, doi: 10.3390/genes13111920.
[13] D. Griffin, R. Feinn, L. Engmann, J. Nulsen, T. Budinetz, and C. Benadiva, ‘Dual trigger with gonadotropin-releasing hormone agonist and standard dose human chorionic gonadotropin to improve oocyte maturity rates’, Fertil. Steril., vol. 102, no. 2, pp. 405–409, Aug. 2014, doi: 10.1016/j.fertnstert.2014.04.028.
[14] S. Hatirnaz et al., ‘Can in vitro maturation overcome cycles with repeated oocyte maturation arrest? A classification system for maturation arrest and a cohort study’, Int. J. Gynaecol. Obstet. Off. Organ Int. Fed. Gynaecol. Obstet., vol. 153, no. 3, pp. 496–502, Jun. 2021, doi: 10.1002/ijgo.13490.