CNSH. Nguyễn Ngọc Trúc Phương, CNSH. Tăng Lê Thái Ngọc, BS. Trương Hữu Duyên
I. Tổng quan về virus trong tinh dịch
Trong những năm gần đây, sự hiện diện của virus trong tinh dịch đã trở thành mối quan tâm đáng kể trong lĩnh vực hỗ trợ sinh sản, khi ngày càng nhiều bằng chứng cho thấy khả năng xâm nhập và tồn tại kéo dài của chúng trong hệ sinh dục. Virus thông qua cơ chế gây viêm và stress oxy hóa từ đó làm rối loạn sinh tinh, suy giảm chất lượng tinh trùng và sự toàn vẹn ADN [1]. Đáng chú ý, một số virus vẫn được phát hiện trong tinh dịch dù xét nghiệm máu đã âm tính, cho thấy nguy cơ lây truyền có thể kéo dài sau giai đoạn hồi phục [2]. Trên cơ sở đó, bài viết này tổng hợp các bằng chứng hiện có về sự hiện diện, tác động của chúng đối với chức năng sinh sản nam và các hướng tiếp cận trong hỗ trợ sinh sản.
II. Phân loại và sự ảnh hưởng của các nhóm virus lên chức năng sinh sản nam
Sự hiện diện của virus trong tinh dịch có thể là hệ quả của nhiều yếu tố khác nhau, bao gồm các con đường lây nhiễm và cơ chế xâm nhập đa dạng vào hệ sinh dục nam. Trên cơ sở đó, việc phân loại các virus dựa trên con đường lây truyền và đặc tính sinh bệnh học là cần thiết nhằm làm rõ vai trò của từng nhóm đối với sức khỏe sinh sản nam.
Virus lây qua đường tình dục
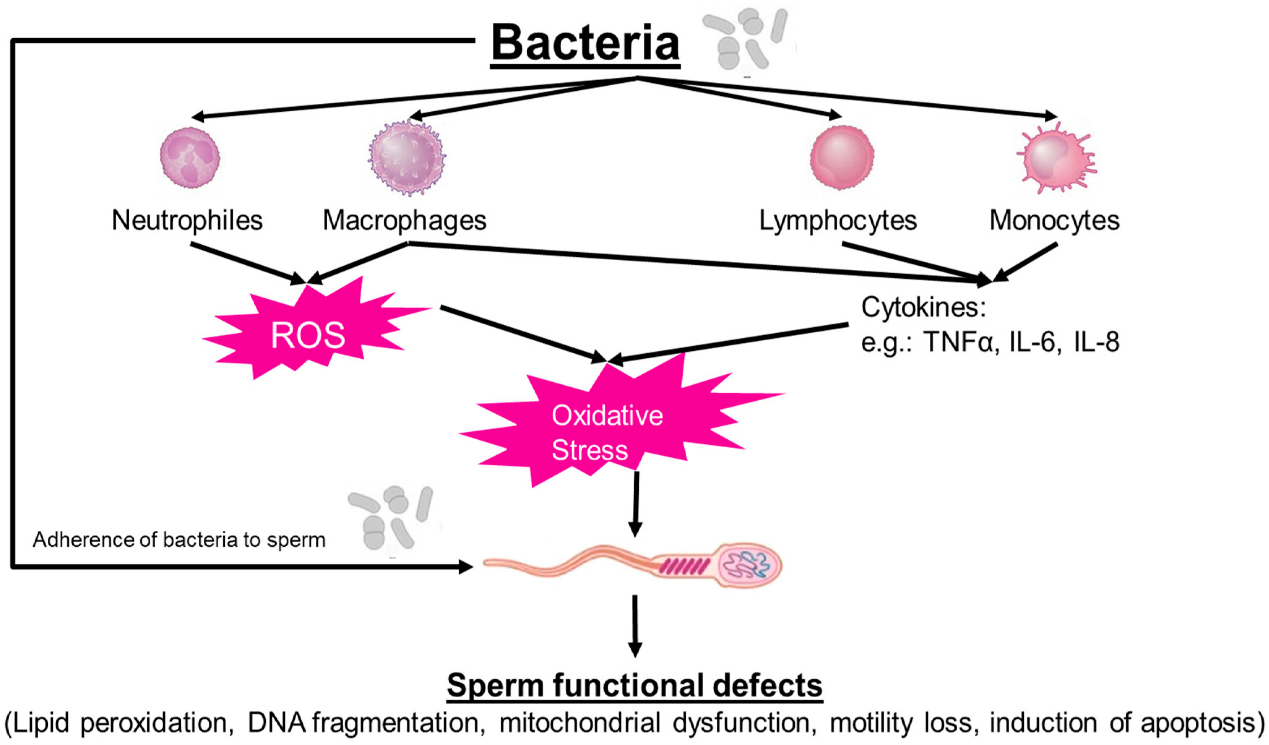
Các virus lây truyền trực tiếp qua đường tình dục như Human Papilloma Virus (HPV), Human Immunodeficiency Virus (HIV) và Hepatitis B Virus (HBV) được đặc trưng bởi khả năng hiện diện tại tinh hoàn, mào tinh, tuyến sinh dục phụ, từ đó gây viêm tại chỗ, stress oxy hoá và tổn thương tế bào sinh tinh [3]. Tuy nhiên, sự suy giảm khả năng sinh sản do từng loại virus gây ra không xuất phát từ một cơ chế đồng nhất, mà phản ánh những khác biệt về vị trí cư trú ưu thế, hình thức tồn tại trong tinh dịch và cơ chế tác động lên tế bào tinh trùng.
Virus u nhú (Human Papilloma Virus - HPV) là đại diện điển hình cho nhóm có khả năng tương tác trực tiếp với tinh trùng. Ở nam giới, virus xâm nhập qua niêm mạc đường sinh dục và khu trú tại nhiều vị trí như niệu đạo, mào tinh, ống dẫn tinh và tinh hoàn [4]. HPV được phát hiện trong tinh dịch với tỉ lệ dao động rộng (0 - 46,2%) và tần suất xuất hiện cao hơn ở nam giới hiếm muộn so với dân số chung (20,4% so với 11,4%, p < 0,001) [5]. Về cơ chế, HPV bám trực tiếp lên tinh trùng thông qua tương tác đặc hiệu giữa các protein capsid L1/L2 của virus và proteoglycan heparan sulfate trên bề mặt tinh trùng, cho phép virus hiện diện và di chuyển cùng tinh trùng trong tinh dịch [6], [7]. Bên cạnh đó, HPV còn hiện diện trong mô tinh hoàn và mào tinh với tỉ lệ hơn 30%, gợi ý khả năng virus xâm nhập tế bào mầm và can thiệp vào quá trình sinh tinh [4]. Trên thực tế, Sun và cộng sự (2025) ghi nhận rằng nhiễm HPV liên quan đến suy giảm chất lượng tinh trùng với các biểu hiện gồm giảm di động, tăng bất thường hình thái và tăng phân mảnh ADN (p < 0,001), phản ánh hệ quả của sự hiện diện virus trong tinh dịch [8].
Virus viêm gan siêu vi B (Hepatitis B Virus - HBV) không chỉ hiện diện trong tinh dịch mà còn vượt qua hàng rào máu - tinh hoàn, xâm nhập trực tiếp vào các tế bào sinh tinh và ảnh hưởng đến ADN tinh trùng. Sau khi xâm nhập, HBV hình thành dạng ADN vòng khép kín cộng hoá trị (covalently closed circular DNA - cccDNA) nhờ gắn với histone trong nhân tế bào chủ để tránh sự đào thải nội bào, giúp virus tồn tại lâu dài [9]. Nhiều nghiên cứu đã phát hiện rằng các kháng nguyên bề mặt của HBV kích hoạt trục Bcl-2/Bax và các yếu tố gây chết tế bào không phụ thuộc caspase làm giảm tỉ lệ sống, khả năng di động và tiềm năng thụ tinh của tinh trùng. Những biến đổi này được chứng minh trong nghiên cứu hồi cứu của Mo và cộng sự (2025) trên 1.566 nam giới hiếm muộn, trong đó 783 trường hợp dương tính HBV. Nhóm dương tính có tỉ lệ di động tiến tới, mật độ tinh trùng thấp hơn (p < 0,05), tỉ lệ tinh trùng bất thường hình thái cao hơn (p < 0,001) và tỉ lệ sống giảm so với nhóm âm tính (p < 0,05), cho thấy HBV làm suy giảm chất lượng tinh trùng [10].
Khác với HPV và HBV, virus gây suy giảm miễn dịch mắc phải ở người (Human Immunodeficiency Virus - HIV) không tác động trực tiếp lên tinh trùng mà ảnh hưởng gián tiếp thông qua rối loạn miễn dịch mạn tính. Trong tinh dịch, virus HIV tồn tại chủ yếu dưới dạng hạt virus tự do hay các tế bào mang virus (lympho, đại thực bào). Sự xâm nhập của HIV phụ thuộc vào tương tác giữa glycoprotein vỏ GP120 và thụ thể CD4⁺ cùng các đồng thụ thể CCR5/CXCR4 trên tế bào chủ. Sau khi xâm nhập, virus có khả năng duy trì nhiễm trùng kéo dài thông qua việc lẩn tránh sự nhận diện của cơ chế miễn dịch nội bào, sao chép ngược và tích hợp bộ gen vào ADN tế bào chủ. Hệ quả của nhiễm HIV kéo dài là sự rối loạn điều hòa cytokine và gia tăng stress oxy hóa tại mô tinh hoàn, dẫn đến viêm tinh hoàn mạn tính và rối loạn chức năng nội tiết. HIV làm suy giảm số lượng và chức năng tế bào Leydig, ảnh hưởng đến vai trò nâng đỡ của tế bào Sertoli, thúc đẩy xơ hóa quanh ống sinh tinh và tổn thương dòng tế bào mầm, từ đó làm giảm hiệu suất sinh tinh [1]. Những biến đổi này góp phần làm suy giảm chất lượng tinh dịch gồm pH, mật độ, khả năng di động tinh trùng, tăng tỉ lệ hình dạng bất thường và tế bào tròn [11]. Nghiên cứu của Savasi và cộng sự (2019) cho thấy các thông số tinh dịch ở bệnh nhân HIV-1 đều giảm đáng kể so với giá trị tham chiếu của WHO (p < 0,001), với mức độ suy giảm tăng theo tải lượng virus (p < 0,05) [12].
Virus khác có thể tồn tại trong tinh dịch
Các nghiên cứu hiện có cho thấy Mumps Virus (MuV), Zika Virus (ZIKV) và SARS-CoV-2 có thể ảnh hưởng đến hệ sinh dục nam như hệ quả thứ phát của nhiễm trùng toàn thân.
Virus quai bị (Mumps Virus - MuV) là tác nhân gây viêm và có thể tiến triển gây teo tinh hoàn ở nam giới [13, 14]. Khi xâm nhập tinh hoàn, MuV khởi phát cơ chế chết tế bào mang tính viêm tại các tế bào Leydig, Sertoli, đại thực bào và tế bào quanh ống sinh tinh thông qua hoạt hóa inflammasome và các caspase viêm, dẫn đến phóng thích mạnh các cytokine tiền viêm như IL-1β. Trong mô hình nuôi cấy mô tinh hoàn, Franklin và cộng sự (2025) ghi nhận MuV nhân lên mạnh, xâm nhiễm tế bào Leydig và đại thực bào mô kẽ ở giai đoạn đầu, sau đó lan sang tế bào Sertoli (p < 0,01) [13]. Đồng thời, nhóm nghiên cứu cũng ghi nhận sự tăng biểu hiện các cytokine gây viêm bao gồm IL-1β, TNF-α, IL-10 và IL-1RA (p < 0,05), sự giảm testosterone, inhibin B và giảm biểu hiện CYP17A1 - enzyme trung tâm trong sinh tổng hợp testosterone (p < 0,05).
Virus Zika là tác nhân đầu tiên không lây qua đường tình dục nhưng được phát hiện trong tinh dịch người và có thể tồn tại kéo dài trên sáu tháng sau nhiễm [15]. Loại virus này có tính hướng đích rõ rệt với tinh hoàn, ưu tiên xâm nhập ống sinh tinh, gây tổn thương, chết tế bào và phá vỡ cấu trúc ống. Ngoài ra, ZIKV xâm nhiễm các tế bào biểu hiện cao thụ thể AXL, bao gồm tế bào Sertoli và đại thực bào, từ đó kích hoạt đáp ứng viêm tại chỗ. Trong nghiên cứu của Vogt và cộng sự (2022), các trường hợp đào thải ZIKV kéo dài ghi nhận tải lượng virus trong tinh dịch cao hơn rõ rệt so với máu (p < 0,001), kèm theo tăng nồng độ cytokine, chemokine và số lượng bạch cầu CD45⁺ trong hai tháng đầu sau khởi phát (p < 0,05) [16]. Đối với chất lượng tinh trùng, Vanegas và cộng sự (2021) đã cung cấp bằng chứng cho thấy nam giới nhiễm ZIKV có tỉ lệ tinh trùng di động giảm, tỉ lệ tinh trùng bất động tăng và mật độ tinh trùng thấp hơn so với nhóm âm tính (p < 0,05) [17].
SARS-CoV-2 là tác nhân được ghi nhận có thể ảnh hưởng đa cơ quan, trong đó hệ sinh sản nam là một đích tác động đáng chú ý. Do COVID-19 ghi nhận nhiều biến đổi mô học tại tinh hoàn như phù mô kẽ, sung huyết, thoát mạch hồng cầu, kèm xâm nhiễm tế bào miễn dịch với sự tăng số lượng bạch cầu CD3⁺, CD68⁺ và nồng độ các cytokine viêm (IL-6, TNF-α, MCP-1). Ngoài ra, SARS-CoV-2 còn gây teo tinh hoàn, chết tế bào dòng mầm và hình thành vi huyết khối trong hệ mạch tinh hoàn [18]. Trong nghiên cứu của Wen và cộng sự (2024) ghi nhận sự suy giảm về thể tích, mật độ và khả năng di động tinh trùng, kèm theo tăng phân mảnh ADN và tăng bạch cầu trong tinh dịch nam giới sau nhiễm (p < 0,05) [19]. Đồng thời, Ashonibare và cộng sự (2024) cho thấy sự rối loạn trục nội tiết sinh sản với sự giảm testosterone và giảm tỉ lệ testosterone/LH, trong khi estradiol và prolactin tăng (p < 0,05), phản ánh sự mất cân bằng điều hòa hormone sinh dục sau nhiễm SARS-CoV-2 [20]. Nhìn chung, mỗi loại virus đều có cơ chế riêng nhưng việc sàng lọc và định hướng chiến lược can thiệp thích hợp vẫn cần thiết để giảm nguy cơ và bảo đảm an toàn cho các kỹ thuật hỗ trợ sinh sản.
III. Hướng tiếp cận trong các kỹ thuật hỗ trợ sinh sản
Trong lâm sàng, khai thác tiền sử bệnh và yếu tố nguy cơ là bước đầu tiên nhằm nhận diện nguy cơ phơi nhiễm. Sàng lọc chủ động thông qua xét nghiệm được thực hiện tiếp theo để phát hiện cả những trường hợp nhiễm không có biểu hiện lâm sàng. Chương trình nghiên cứu của Oliveira và cộng sự (2024) về các bệnh lây qua đường tình dục đã được triển khai tại một trường đại học nhằm đánh giá khả năng phát hiện sớm các trường hợp nhiễm không triệu chứng ở quần thể người trẻ. Nhóm tác giả ghi nhận khoảng 13% người tham gia nhiễm ít nhất một tác nhân gây bệnh, trong đó phần lớn không có biểu hiện tại thời điểm xét nghiệm. Đáng chú ý, các virus lây truyền qua đường tình dục như HIV, viêm gan B và C vẫn được phát hiện dù tỉ lệ thấp, cho thấy nguy cơ nhiễm virus có thể tồn tại âm thầm [21]. Một nghiên cứu khác của Depuydt và cộng sự (2018) ghi nhận tỉ lệ phát hiện HPV trong mẫu ngân hàng tinh trùng dao động từ 3,1% đến 16,7%. Khi phân tích kết quả lâm sàng, mẫu tinh trùng dương tính HPV không ghi nhận trường hợp mang thai lâm sàng nào, trái lại mẫu âm tính đạt tỉ lệ mang thai khoảng 14,6% [22]. Những phát hiện này củng cố vai trò thiết yếu của việc sàng lọc chủ động, qua đó tạo cơ sở cho các bước điều trị theo phác đồ chuẩn, tư vấn và can thiệp dự phòng phù hợp.
Trong hỗ trợ sinh sản, việc chuẩn hoá quy trình chuẩn bị tinh trùng nhằm mục đích hạn chế tối đa sự hiện diện virus trong mẫu tinh dịch. Các kỹ thuật phổ biến như ly tâm thang nồng độ và swim-up giúp loại bỏ tinh tương, tế bào miễn dịch và phần lớn các virus tồn tại ở dạng tự do hoặc chỉ gắn lỏng lẻo trên bề mặt tinh trùng [23]. Hiệu quả của các phương pháp này đã được chứng minh trong nghiên cứu của Carvalho và cộng sự (2021) trên 180 chu kỳ IUI của các cặp vợ chồng có người chồng dương tính HIV. Tinh trùng trước khi sử dụng được xử lý bằng quy trình lọc rửa kết hợp ly tâm thang nồng độ và swim-up, sau đó được xét nghiệm HIV bằng PCR để xác nhận âm tính trước khi tiến hành IUI. Kết quả ghi nhận 16 trường hợp mang thai, tương ứng tỉ lệ 9,0% mỗi chu kỳ và không ghi nhận trường hợp lây nhiễm HIV ở phụ nữ hay trẻ sơ sinh trong thời gian theo dõi [24]. Bên cạnh các kỹ thuật chuẩn bị tinh trùng, một số nghiên cứu cũng đề xuất các chiến lược xử lý nâng cao nhằm loại bỏ virus bám trên tinh trùng. Nghiên cứu của Toni và cộng sự (2021) ghi nhận tỉ lệ tinh trùng mang HPV-ADN trung bình 17,1 ± 10,5% ở các bệnh nhân có tinh dịch dương tính HPV. Phân tích trên FISH cho thấy virus bám trên bề mặt đầu tinh trùng tại các vùng giàu glycosaminoglycans (GAGs). Dựa trên cơ chế này, nhóm tác giả đã sử dụng hyaluronidase nhằm thủy phân các GAGs bề mặt, phá vỡ liên kết giữa HPV và đầu tinh trùng. Sau khi xử lý tinh dịch bằng hyaluronidase (80 IU/mL) kết hợp swim-up, toàn bộ mẫu đều âm tính với HPV-ADN khi đánh giá lại bằng FISH và INNO-LiPA [25].
Bên cạnh đó, trong bối cảnh virus gây tổn thương trực tiếp mô tinh hoàn và đe dọa khả năng sinh tinh, các chiến lược xâm lấn có thể được cân nhắc. Trong đó, vi phẫu trích tinh trùng từ mô tinh hoàn (Microdissection Testicular Sperm Extraction - microTESE) kết hợp ICSI được xem là một hướng tiếp cận hiệu quả. Nghiên cứu của Nguyen Phan và cộng sự (2024) cho thấy mặc dù bệnh nhân có tiền sử viêm tinh hoàn do nhiễm MuV đối mặt với nguy cơ vô tinh cao, kết quả điều trị bằng chiến lược microTESE - ICSI ở nhóm này vẫn cho kết quả thụ tinh cao hơn so với nhóm vô tinh không bế tắc (66,1% so với 57,7%; p < 0,01). Đồng thời, nhóm này ghi nhận tỉ lệ phôi tốt ngày 3, phôi nang ngày 5, tỉ lệ có thai sinh hóa, thai tiến triển và trẻ sinh sống cao hơn hoặc tương đương so với nhóm chứng (p < 0,05) [26].
Các dữ liệu trên cho thấy tinh dịch có vai trò đặc biệt trong bối cảnh nhiễm virus. Điều này đặt ra yêu cầu phải đánh giá cẩn trọng nguy cơ lây truyền và tác động đến kết cục sinh sản trong thực hành lâm sàng.
IV. Kết luận
Nhiễm virus trong tinh dịch là yếu tố có thể ảnh hưởng đáng kể đến sức khỏe sinh sản nam thông qua nhiều cơ chế. Sự hiện diện của virus dù bắt nguồn từ cơ chế nào cũng đều làm thay đổi chất lượng tinh dịch. Khi áp dụng các kỹ thuật hỗ trợ sinh sản, việc nhận diện, xử lý và theo dõi các mẫu tinh dịch nhiễm virus là cần thiết để bảo đảm an toàn và duy trì hiệu quả điều trị. Tuy nhiên, bằng chứng hiện tại vẫn chưa đồng nhất và còn thiếu dữ liệu dài hạn, cho thấy nhu cầu tiếp tục nghiên cứu để hiểu rõ hơn tác động của từng loại virus và hoàn thiện các chiến lược can thiệp phù hợp trong thực hành lâm sàng.
TÀI LIỆU THAM KHẢO
1. Akhigbe R.E., Dutta S., Hamed M.A., et al. (2022). Viral Infections and Male Infertility: A Comprehensive Review of the Role of Oxidative Stress. Front Reprod Health, 4.
2. Update on known and emergent viruses affecting human male genital tract and fertility | Basic and Clinical Andrology | Springer Nature Link.
3. Guo Y., Dong Y., Zheng R., et al. (2024). Correlation between viral infections in male semen and infertility: a literature review. Virol J, 21(1), 167.
4. Isaguliants M., Krasnyak S., Smirnova O., et al. (2021). Genetic instability and anti-HPV immune response as drivers of infertility associated with HPV infection. Infect Agents Cancer, 16(1), 29.
5. Lyu Z., Feng X., Li N., et al. (2017). Human papillomavirus in semen and the risk for male infertility: a systematic review and meta-analysis. BMC Infect Dis, 17, 714.
6. Foresta C., Patassini C., Bertoldo A., et al. (2011). Mechanism of Human Papillomavirus Binding to Human Spermatozoa and Fertilizing Ability of Infected Spermatozoa. PLoS One, 6(3), e15036.
7. Horvath C.A., Boulet G.A., Renoux V.M., et al. (2010). Mechanisms of cell entry by human papillomaviruses: an overview. Virol J, 7(1), 11.
8. Sun H., Tang X., Tong L., et al. (2025). Retrospective analysis of the impact of human papillomavirus infection in the male genital tract on sperm: from a single center. Front Cell Infect Microbiol, 15.
9. Wei L. and Ploss A. (2021). Hepatitis B virus cccDNA is formed through distinct repair processes of each strand. Nat Commun, 12(1), 1591.
10. Mo Y., Liang F., Wei H., et al. (2025). Hepatitis B virus infection is associated with impaired sperm quality: a retrospective cohort study of 1566 infertile men. Middle East Fertil Soc J, 30(1), 34.
11. Nicopoullos J.D.M., Almeida P.A., Ramsay J.W.A., et al. (2004). The effect of human immunodeficiency virus on sperm parameters and the outcome of intrauterine insemination following sperm washing. Hum Reprod, 19(10), 2289–2297.
12. Savasi V., Parisi F., Oneta M., et al. (2019). Effects of highly active antiretroviral therapy on semen parameters of a cohort of 770 HIV-1 infected men. PLoS One, 14(2), e0212194.
13. Wu H., Wang F., Tang D., et al. (2021). Mumps Orchitis: Clinical Aspects and Mechanisms. Front Immunol, 12.
14. Mumps virus infection triggers early pro-inflammatory responses and impairs Leydig and Sertoli cell function in an ex vivo human testis model | Human Reproduction | Oxford Academic.
15. Liu H., Geng C.-H., Wang W., et al. (2013). [Effects of hepatitis B virus on human semen parameters and sperm DNA integrity]. Zhonghua Nan Ke Xue, 19(10), 896–898.
16. Vogt M.B., McDonald E.M., Delorey M., et al. (2022). Association Between Prolonged Shedding of Zika Virus in Human Semen and Male Reproductive Tract Inflammation. J Infect Dis, 226(7), 1140–1150.
17. Vanegas H., González F., Reyes Y., et al. (2021). Zika RNA and Flavivirus-Like Antigens in the Sperm Cells of Symptomatic and Asymptomatic Subjects. Viruses, 13(2).
18. Flaifel A., Guzzetta M., Occidental M., et al. (2021). Testicular Changes Associated With Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2). Arch Pathol Lab Med, 145(1), 8–9.
19. Wen L., Tian H., Huang X., et al. Effect of SARS-CoV-2 on semen parameters: A meta-analysis of 39 articles from 15 countries. J Glob Health, 14, 05021.
20. J A.V., J A.P., M A.T., et al. (2024). SARS-CoV-2 impairs male fertility by targeting semen quality and testosterone level: A systematic review and meta-analysis. PLOS ONE, 19(9), e0307396.
21. Oliveira J.M., Martins A.H., Veiga D., et al. (2024). Screening for STIs: Results of a Health-Promotion Programme in a Portuguese University. Microorganisms, 12(12).
22. Depuydt* C., Donders G., Verstraete L., et al. Time has come to include Human Papillomavirus (HPV) testing in sperm donor banks. Facts Views Vis Obgyn, 10(4), 201–205.
23. Van der Kuyl A.C. and Berkhout B. (2020). Viruses in the reproductive tract: On their way to the germ line?. Virus Research, 286, 198101.
24. Prevention of HIV transmission with sperm washing within fertile serodiscordant couples undergoing non-stimulated intrauterine insemination: AIDS Care: Vol 33, No 4.
25. Hyaluronidase-based swim-up for semen selection in patients with human papillomavirus semen infection | Biology of Reproduction | Oxford Academic.
26. Nguyen Phan T., Lai V.T.T., Dinh V.H., et al. (2024). P-078 Comparison of embryological and clinical outcomes in mumps orchitis and non-obstructive azoospermia patients treated by Microdissection testicular sperm extraction combined with ICSI (microTESE-ICSI). Hum Reprod, 39.