CNSH. Quảng Thị Phước Tín1, ThS. Bs. Dương Công Bằng1
Bệnh viện Phụ sản Quốc tế Sài Gòn
- Giới thiệu
Nhiễm khuẩn tinh dịch (bacteriospermia) và gia tăng bạch cầu (leukocytospermia) được xác định là những tác nhân chính làm suy giảm chất lượng tinh trùng thông qua stress oxy hóa, phản ứng viêm và rối loạn thành phần cytokine. Hệ quả trực tiếp là gia tăng phân mảnh ADN tinh trùng (Sperm DNA Fragmentation - SDF) ngay cả ở nam giới có chỉ số tinh dịch đồ (TDĐ) bình thường (normozoospermic) [1], [2].
Bacteriospermia chiếm tỷ lệ đáng kể, từ 15 - 70% ở nam giới khám hiếm muộn [1],[2]. Trong đó các bệnh lý nhiễm trùng là nguyên nhân ở khoảng 15% các trường hợp vô sinh do nam. Mức độ ảnh hưởng của bacteriospermia phụ thuộc vào tải lượng và sự đa dạng vi khuẩn trong tinh dịch [3]. Điều này phản ánh ranh giới giữa vi khuẩn cộng sinh vô hại và tình trạng nhiễm trùng không triệu chứng gây độc cho tinh trùng.
Bacteriospermia được định nghĩa là sự hiện diện của vi khuẩn trong tinh dịch vượt ngưỡng sinh lý (≥103 CFU/mL). Đáng chú ý, có tới 67% nam giới có kết quả tinh dịch bị nhiễm khuẩn nhưng hoàn toàn không có triệu chứng lâm sàng rõ rệt do tải lượng vi khuẩn đủ để gây hại cho tinh trùng nhưng chưa đủ để kích hoạt phản ứng viêm toàn thân gây sốt hoặc đau cấp tính [2]. Sự hiện diện âm thầm của vi khuẩn làm biến đổi môi trường vi mô của tinh dịch, tổn thương ADN tinh trùng và tác động trực tiếp đến kết quả của kỹ thuật tiêm tinh trùng vào bào tương noãn (Intracytoplasmic Sperm Injection - ICSI) [1],[2].
- Hệ vi sinh vật trong tinh dịch và nguồn gốc vi khuẩn
Trong điều kiện sinh lý, sự cân bằng hệ sinh thái nội môi (ecological homeostasis) của các vi sinh vật cộng sinh trong tinh dịch đóng vai trò quan trọng trong việc duy trì sức khỏe sinh sản nam giới, thường chiếm ưu thế bởi các chủng Lactobacillus, Corynebacterium và Staphylococcus. Tuy nhiên, khi mất cân bằng vi sinh (dysbiosis), sự xâm nhập và phát triển quá mức của các tác nhân gây bệnh như Escherichia coli, Enterococcus faecalis, Chlamydia trachomatis hoặc Ureaplasma urealyticum có thể kích hoạt phản ứng viêm, sản sinh gốc oxy hóa và các cơ chế gây tổn thương tinh trùng, từ đó làm suy giảm chức năng sinh sản nam giới [4],[5].
Vi khuẩn hiện diện trong tinh dịch có thể đến từ nhiều nguồn:
- Nguồn gốc nội sinh: khoảng 30% vi sinh vật có từ niệu đạo, trong khi các chi như Pseudomonas và Acidovorax chủ yếu bắt nguồn từ tuyến tiền liệt và túi tinh [4].
- Hoạt động tình dục: hoạt động tình dục đóng vai trò là một nguồn trao đổi vi sinh vật cộng sinh trong đường sinh dục, chiếm khoảng 56 - 61% các chi vi khuẩn tồn tại nơi đây [4]. Các bệnh lây truyền qua đường tình dục (Sexually Transmitted Infections - STIs) như HPV, Chlamydia và lậu cũng xâm nhập qua con đường này, gây ra tình trạng chết theo chương trình và tổn thương ADN [3],[4].
- Ngoại nhiễm: trong quá trình thu thập mẫu, vi khuẩn từ bề mặt da như Staphylococcus hoặc từ bàn tay có thể xâm nhập vào mẫu tinh dịch. Các biện pháp vệ sinh nghiêm ngặt trước khi lấy mẫu giúp tránh sai lệch kết quả chẩn đoán [2],[6].
- Trục ruột - tinh hoàn: chế độ ăn uống và tình trạng béo phì có thể ảnh hưởng đến vi khuẩn tinh dịch thông qua trục ruột - tinh hoàn. Tình trạng loạn khuẩn đường ruột do chế độ ăn nhiều chất béo có thể dẫn đến sự thay đổi nồng độ các vi khuẩn như Bacteroidetes và Prevotella trong tinh dịch, tương quan trực tiếp với sự suy giảm mật độ và khả năng vận động của tinh trùng [4].
Phân loại hệ vi sinh vật trong tinh dịch:
- Vi khuẩn Gram âm: như Escherichia coli và Klebsiella pneumoniae thường liên quan đến giảm mật độ, khả năng di động và gây ngưng kết tinh trùng [5],[7].
- Vi khuẩn Gram dương: nhóm vi khuẩn có lợi như Lactobacillus giúp duy trì độ pH bảo vệ tinh trùng, trong khi các loại gây bệnh như Enterococcus faecalis gây viêm nhiễm và có tỷ lệ kháng kháng sinh cao [5],[8].
- Nhiễm khuẩn tinh dịch và tình trạng bạch cầu trong tinh dịch (Leukocytospermia)
Nhiễm khuẩn tinh dịch thường kích hoạt phản ứng viêm tại chỗ, dẫn đến có bạch cầu trong tinh dịch (chiếm khoảng 10% các trường hợp bacteriospermia và 30% vô sinh nam) [2]. Sự hiện diện đồng thời của bacteriospermia và leukocytospermia phản ánh nguyên nhân gây viêm tại đường sinh dục nam, làm thay đổi thành phần cytokine và tăng sinh các gốc oxy hóa tự do trong tinh dịch [1].
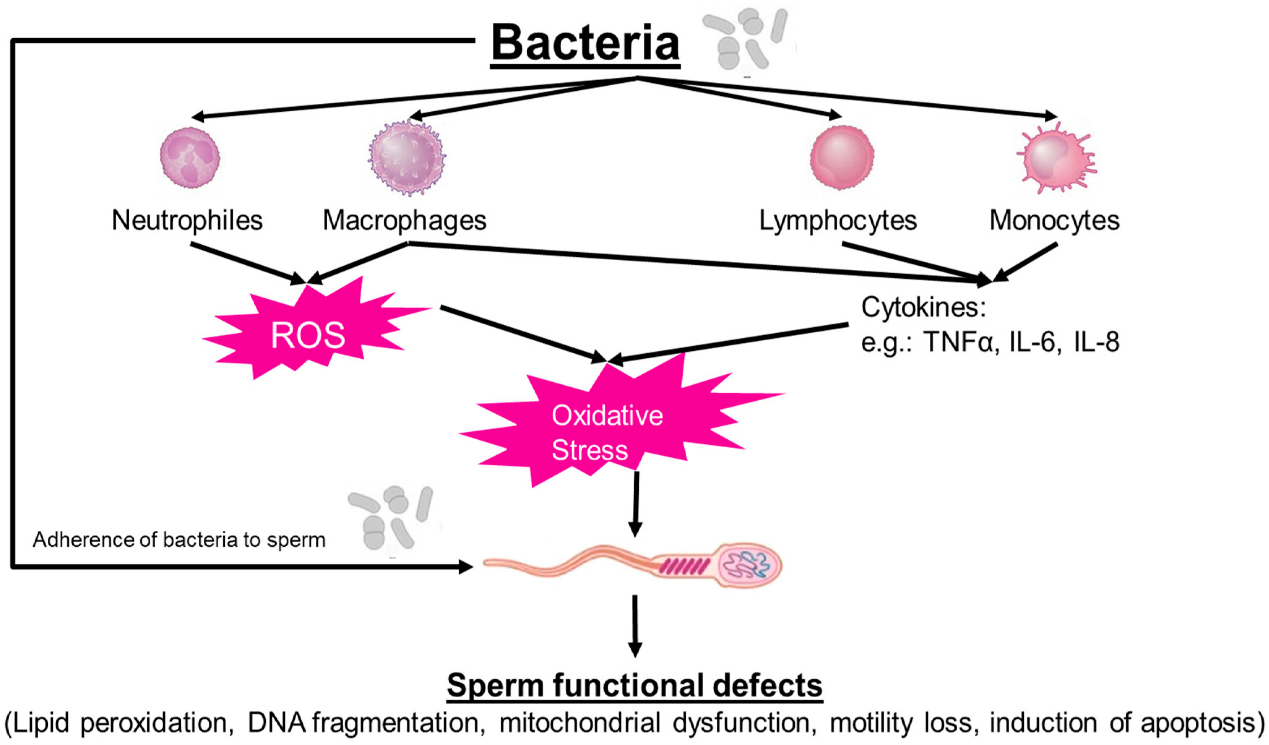
Nhiễm khuẩn gây thay đổi nồng độ các dấu ấn viêm trong tinh tương, đặc trưng bởi sự gia tăng của các cytokine tiền viêm như IL-6, IL-8 và TNF-α. Các phân tử tín hiệu này không chỉ gây độc trực tiếp cho tinh trùng mà còn làm suy yếu hệ thống chống oxy hóa nội sinh và tạo nên tình trạng viêm mạn tính [1]. Sự xâm nhiễm bạch cầu gây giải phóng các gốc tự do (Reactive Oxygen Species - ROS) và dẫn đến tổn thương các vi cấu trúc, giảm khả năng sống của tinh trùng [9],[10].
- Cơ chế phân tử gây tổn thương tinh trùng và phân mảnh ADN
Nhiễm khuẩn tinh dịch gây tổn thương ADN thông qua các cơ chế sau:
- Stress oxy hóa và sự hình thành ROS: kích hoạt các bạch cầu đa nhân trung tính (Polymorphonuclear neutrophils - PMN) giải phóng ROS để tiêu diệt vi khuẩn. Tuy nhiên, lượng ROS dư thừa sẽ tấn công màng tinh trùng giàu axit béo chưa bão hòa (Polyunsaturated Fatty Acids - PUFA), gây peroxy hóa lipid, làm suy giảm tính toàn vẹn màng, rối loạn chức năng ty thể và giảm khả năng di động [3].
- Tương tác trực tiếp và sự bám dính tế bào: Vi khuẩn như Escherichia coli sử dụng các cấu trúc bề mặt (pili hoặc fimbriae) để bám dính trực tiếp lên màng tinh trùng, đóng vai trò như cầu nối sinh học gây ngưng kết tinh trùng (agglutination), làm giảm khả năng di động và gây tổn thương cơ học cho màng tế bào [2]. Sự kết hợp giữa bám dính cơ học và stress oxy hóa tại chỗ làm gia tăng thêm các tổn thương nội bào, đặc biệt là SDF.
- Phản ứng acrosome sớm (sAR): các tác nhân như Escherichia coli và Pseudomonas aeruginosa kích hoạt phản ứng acrosome sớm, làm gián đoạn quá trình khả năng hóa tinh trùng (capacitation) bằng cách ức chế dòng Ca2+, hoạt hóa con đường Protein Kinase A (PKA) và phosphoryl hóa tyrosine, dẫn đến rối loạn polyme hóa actin và phá vỡ lớp vỏ F-actin bảo vệ, hệ quả là màng acrosome trở nên không ổn định và dễ vỡ sớm. Azoulay và cộng sự (2023) chỉ ra rằng sAR khiến tinh trùng mất khả năng thụ tinh tự nhiên. Đáng lưu ý, trong kỹ thuật ICSI, việc màng acrosome không ổn định có thể giải phóng các enzyme thủy phân và độc tố sớm, gây độc cho bào tương noãn và ảnh hưởng đến sự phát triển của hợp tử. Tuy nhiên, sự tăng nồng độ cAMP nội bào có thể đảo ngược hiện tượng này, gợi mở tiềm năng can thiệp nhằm phục hồi chức năng tinh trùng [11].
- Cơ chế đứt gãy ADN: ADN tinh trùng được bảo vệ bởi protamine, nhưng khi nhiễm khuẩn, ROS từ vi khuẩn và bạch cầu gây stress oxy hóa vượt quá khả năng trung hòa của tinh trùng và có thể phá vỡ hàng rào bảo vệ này [2]. ROS tấn công trực tiếp vào các bazơ nitơ hoặc khung đường–phosphate, gây đứt gãy chuỗi đơn (single-strand breaks). Nghiêm trọng hơn, đứt gãy chuỗi kép (double-strand breaks) hình thành do rối loạn quá trình sửa chữa ADN hoặc do apoptosis được kích hoạt bởi vi khuẩn, độc tố và cytokine viêm, liên quan đến rối loạn chức năng ty thể và hoạt hóa nuclease [3]. Các nghiên cứu khác cũng khẳng định nhiễm khuẩn làm suy giảm đáng kể tính toàn vẹn ADN, dẫn đến tỷ lệ SDF cao ở nam giới hiếm muộn [9],[10].
- Phản ứng viêm và thành phần cytokine tinh dịch: Nhiễm khuẩn làm thay đổi thành phần cytokine trong tinh dịch, đặc biệt là các cytokine tiền viêm IL-6, IL-8 và TNF-α. Nồng độ các cytokine này tăng cao, ảnh hưởng tiêu cực đến mật độ, độ di động và khả năng sống của tinh trùng. Trong đó IL-8 có vai trò hóa hướng động thu hút bạch cầu, còn IL-6 và TNF-α liên quan đến phân mảnh ADN tinh trùng và apoptosis [2]. Sự gia tăng cytokine đi kèm với tăng ROS, gây peroxide hóa lipid màng và tổn thương ADN, phản ánh tình trạng viêm kéo dài và gây rối loạn chức năng tinh trùng [9].
- Ảnh hưởng của nhiễm khuẩn tinh dịch đến kết cục tạo phôi sau ICSI
- Tác động lên thông số tinh dịch: những thất bại sau ICSI bắt nguồn từ sự suy giảm nghiêm trọng các thông số sinh học của tinh trùng do nhiễm khuẩn tinh dịch. Nhiễm khuẩn làm giảm mật độ, độ di động và tỷ lệ sống của tinh trùng. Nam giới bị nhiễm khuẩn tinh dịch thường có chỉ số phân mảnh ADN (DNA Fragmentation Index - DFI) cao hơn đáng kể (từ 15-25%, đôi khi lên tới 40%) và độ di động <30%. Hiện tượng ngưng kết có thể ảnh hưởng từ 40 - 75% lượng tinh trùng di động, gây khó khăn trong việc lựa chọn giao tử. Những tổn thương này còn bao gồm cả sự suy giảm điện thế màng ty thể và khởi phát sớm quá trình chết theo chương trình [8],[10].
- Giảm tỷ lệ thụ tinh và chất lượng phôi: Các nghiên cứu cho thấy sự hiện diện của vi khuẩn làm giảm đáng kể tỷ lệ thụ tinh, đặc biệt khi đi kèm với sự gia tăng SDF. Cụ thể, đối với mỗi 1% tăng thêm của DFI, khả năng đạt được tỷ lệ thụ tinh tối ưu (>80%) sẽ giảm đi 1,6%. Mức độ ảnh hưởng còn phụ thuộc vào chủng vi khuẩn gây nhiễm, Streptococcus agalactiae cho tỷ lệ thụ tinh lên tới 94,79%, còn các chủng nguy hiểm như Klebsiella pneumoniae có thể làm giảm tỷ lệ thụ tinh xuống mức rất thấp 18,18% [12].
Dù có thể sử dụng cho ICSI, nhưng tinh trùng từ mẫu tinh dịch bị nhiễm khuẩn vẫn mang theo các tổn thương ADN vào hợp tử. Hợp tử có thể phát triển bình thường trong 2 ngày đầu (nhờ cơ chế sửa chữa của noãn). Nhưng đến ngày thứ 3, giai đoạn kích hoạt bộ gen từ người cha, các phôi có nguồn gốc từ tinh trùng phân mảnh ADN thường có xu hướng chậm phát triển, phân chia bất thường hoặc ngừng phát triển trước giai đoạn phôi nang [13].
- Rủi ro trong chọn lọc tinh trùng: Trong ICSI, lựa chọn tinh trùng dựa trên hình thái bên ngoài và những tinh trùng có hình thái bình thường vẫn có thể mang ADN bị phân mảnh do tác động của vi khuẩn mà kính hiển vi thường không thấy được [2]. Việc tiêm những tinh trùng này, làm tăng nguy cơ phôi ngừng phát triển hoặc sảy thai sớm [9]. Do hiện tượng ngưng kết và bất động nên việc tìm kiếm tinh trùng di động tốt trong mẫu nhiễm khuẩn rất khó khăn, dẫn đến nguy cơ chọn những tinh trùng kém chất lượng [3]. Ngoài ra, vi khuẩn hoặc độc tố bám dính trên màng tinh trùng có thể vô tình được đưa vào trong tế bào chất của noãn trong quá trình tiêm, gây ảnh hưởng đến sự sống của phôi.
- Thất bại làm tổ và sảy thai liên tiếp: Thực hiện ICSI từ các mẫu nhiễm làm tăng đáng kể các rủi ro về thai kỳ và sức khỏe thế hệ sau do bỏ qua hàng rào chọn lọc tự nhiên [2],[9]. Đặc biệt, nhiễm Escherichia coli trong môi trường nuôi cấy hoặc mẫu tinh trùng làm tăng nguy cơ sảy thai sớm [12]. Nhiễm khuẩn còn có thể lây nhiễm vào môi trường nuôi cấy hoặc gây viêm nội mạc tử cung gián tiếp nếu không được xử lý. Kết cục là tỷ lệ thai lâm sàng giảm đáng kể (từ 50,29% xuống còn 42,91%) và tỷ lệ sảy thai tăng cao (lên đến 17,42%) ở những cặp đôi có người chồng bị nhiễm khuẩn tinh dịch nhưng không được điều trị. Tình trạng này được giải thích là do vi khuẩn thúc đẩy quá trình stress oxy hóa và đứt gãy ADN tinh trùng, dẫn đến những tổn thương nghiêm trọng đối với sự phát triển của hợp tử và phôi [2],[12].
Đáng lo ngại hơn, các biến đổi thượng di truyền và đứt gãy ADN sợi đôi (Double-Strand Breaks - DSB) thường không được hệ thống sửa chữa của noãn xử lý hoàn toàn trong quá trình ICSI. Việc bỏ qua các hàng rào chọn lọc tự nhiên này dẫn đến nguy cơ di truyền các khiếm khuyết vào hợp tử. Những khiếm khuyết này không chỉ gây ra các bất thường về hình thái trong giai đoạn phôi thai, mà còn tái lập trình các con đường chuyển hóa và phát triển của thai nhi. Hệ quả là trẻ sinh ra có thể phải đối mặt với các rối loạn về chuyển hóa, suy giảm chức năng nội tiết và các vấn đề về sức khỏe sinh sản khi trưởng thành [4],[9].
- Nhận diện mẫu có nguy cơ nhiễm khuẩn cao tại labo
Việc nhận diện sớm các mẫu tinh dịch có nguy cơ nhiễm khuẩn thông qua các dấu hiệu đại thể và vi thể:
- Tăng độ nhớt và giảm các thông số tinh dịch: độ nhớt tinh dịch là một dấu hiệu đại thể quan trọng giúp nhận diện nguy cơ nhiễm khuẩn tinh dịch và tình trạng viêm tại đường sinh dục nam, thường đi kèm với những tác động tiêu cực đến chất lượng mẫu. Sự hiện diện của vi khuẩn kích hoạt phản ứng viêm dẫn đến các thay đổi bất thường như tăng độ nhớt, thường xuất hiện đồng thời với hiện tượng ngưng kết và vi khuẩn bám dính [3]. Đây là biểu hiện lâm sàng điển hình của viêm các tuyến sinh dục phụ, thường liên quan chặt chẽ đến tình trạng tăng bạch cầu trong tinh dịch và có mối liên hệ với sự suy giảm các đặc điểm chức năng của tinh trùng [2].
- Ngưng kết tinh trùng: Hiện tượng ngưng kết tinh trùng (agglutination) được xác định là một cơ chế gây hại trực tiếp của nhiễm khuẩn, trong đó Fraczek và cộng sự (2015) đã làm rõ tác động của vi khuẩn Escherichia coli (E. coli) với khả năng bám dính lên màng tế bào, khiến các tinh trùng dính kết lại với nhau và làm bất động chúng [3].
Cơ chế vi khuẩn gây ngưng kết tinh trùng diễn ra thông qua sự kết hợp giữa tương tác bám dính trực tiếp và các phản ứng sinh hóa gián tiếp. Các vi khuẩn như E.coli sử dụng những cấu trúc bề mặt đặc hiệu (pili hoặc fimbriae) để gắn vào thụ thể trên màng tinh trùng, đóng vai trò như các “cầu nối sinh học” liên kết các tế bào và gây bất động cơ học [3]. Song song với đó, phản ứng miễn dịch kích hoạt thành phần cytokine trong tinh dịch, dẫn đến tăng bạch cầu và giải phóng các gốc tự do (ROS) gây stress oxy hóa [2].
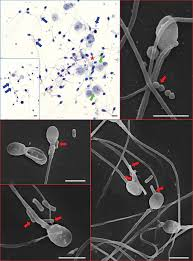
Hình 1. Tương tác giữa vi khuẩn, bạch cầu và tinh trùng người [4]
Chú thích: Tiêu bản nhuộm Papanicolaou của tinh dịch người với hiện tượng nhiễm khuẩn tinh dịch và bạch cầu tinh dịch tại chỗ. Sự ngưng kết tinh trùng khi có mặt vi khuẩn (dấu sao), sự bám dính của vi khuẩn (mũi tên xanh dương) và bạch cầu (mũi tên xanh lá cây) vào cấu trúc tinh trùng (A, B). Ảnh hiển vi điện tử quét của tinh trùng người được xuất tinh và cấy với Bacteroides ureolyticus (C) hoặc với Escherichia coli, serotype O75:HNT (D–F) trong điều kiện in vitro. Sự bám dính của vi khuẩn vào cấu trúc tinh trùng (mũi tên đỏ).
- Khó khăn trong xử lý mẫu: Sự liên kết bền vững giữa vi khuẩn và tinh trùng gây khó khăn cho các kỹ thuật lọc rửa thông thường (như gradient thang nồng độ), vì vi khuẩn bám dính sẽ cùng lắng xuống với tinh trùng thay vì bị tách bỏ và làm giảm chất lượng mẫu [2]. Những đặc điểm này không chỉ gây khó khăn về mặt kỹ thuật mà còn phản ánh tình trạng bệnh lý liên quan đến tổn thương ADN và giảm khả năng sống của tinh trùng [9],[10].
Bên cạnh các dấu hiệu đại thể truyền thống, xu hướng nghiên cứu hiện đại đang chuyển dịch sang việc ứng dụng công nghệ giải trình tự gene thế hệ mới (Next-Generation Sequencing - NGS) và metagenomics. Phương pháp này cho phép mô tả toàn diện hệ vi sinh vật tinh dịch (semen microbiome) và phát hiện chính xác các chủng vi khuẩn mà phương pháp nuôi cấy cổ điển thường bỏ sót, từ đó mở ra cái nhìn sâu sắc hơn về mối liên hệ giữa sự mất cân bằng vi sinh và các tổn thương tinh trùng [6],[13].
- Chẩn đoán và chiến lược can thiệp
Bước tiên quyết để chẩn đoán chính xác và quản lý hiệu quả bacteriospermia là phân biệt giữa bạch cầu và tế bào tròn (tế bào dòng tinh) trong xét nghiệm TDĐ. Việc nhuộm peroxidase hoặc sử dụng xét nghiệm sinh hóa nhanh giúp tránh nhầm lẫn giữa hai loại tế bào này, từ đó định hướng điều trị đúng và tránh lạm dụng kháng sinh. Bạch cầu là nguồn sản sinh ROS chính (gấp 100 lần so với tinh trùng) gây stress oxy hóa và tổn thương màng tế bào [2]. Sự hiện diện của ROS thường báo hiệu nhiễm khuẩn và liên quan trực tiếp đến gia tăng đứt gãy ADN, ảnh hưởng tiêu cực đến khả năng thụ tinh [9],[10]. Do đó, phân biệt đúng hai loại tế bào này giúp định hướng điều trị kháng sinh hiệu quả thay vì bỏ sót nguyên nhân gây viêm [3],[7].
Việc ứng dụng NGS hoặc metagenomics là cần thiết để đánh giá tình trạng loạn khuẩn trong tinh dịch. Về chiến lược điều trị, liệu pháp kháng sinh dựa trên kháng sinh đồ là phương pháp giúp cải thiện đáng kể các thông số tinh dịch và giảm DFI [7],[9],[14]. Do cơ chế gây hại chủ yếu liên quan đến stress oxy hóa nên cần phối hợp điều trị kháng sinh với các liệu pháp chống oxy hóa để bảo vệ toàn vẹn màng và ADN tinh trùng [2],[10]. Việc bổ sung các chất chống oxy hóa (Antioxidant) như: vitamin C, E, Zn và L-carnitine giúp giảm tải lượng ROS và cải thiện độ toàn vẹn ADN [7]. Song song đó, bệnh nhân cần kiểm soát các yếu tố môi trường và lối sống để tối ưu hóa hiệu quả điều trị. Trong thụ tinh trong ống nghiệm, việc xử lý mẫu kỹ lưỡng để loại bỏ vi khuẩn bám dính và điều trị dứt điểm viêm nhiễm là bắt buộc để ngăn ngừa rủi ro thất bại làm tổ và sảy thai [3],[7].
Ngoài ra, việc ứng dụng các kỹ thuật tiên tiến như MACS (Microfluidic sperm sorting) và vi lưu (Microfluidics) giúp loại bỏ các tinh trùng apoptosis và chứa ADN phân mảnh. Các phương pháp này giúp giảm thiểu các tác động cơ học sinh thêm ROS nhân tạo so với ly tâm truyền thống, đồng thời ngăn chặn vi khuẩn kích hoạt phản ứng acrosome tự phát, đảm bảo khả năng thụ tinh khi tiêm vào noãn [2],[11].
- Kết luận và khuyến nghị
Nhiễm khuẩn tinh dịch (bacteriospermia) là một nguyên nhân gây vô sinh nam, không chỉ làm suy giảm các thông số TDĐ cơ bản, mà còn gây ra những tổn thương nghiêm trọng ở cấp độ phân tử. Thông qua stress oxy hóa và phản ứng viêm, bacteriospermia dẫn đến tăng tỷ lệ phân mảnh ADN và kích hoạt apoptosis, ngay cả ở những nam giới normozoospermic. Đáng chú ý, vi khuẩn còn có khả năng kích hoạt phản ứng acrosome tự phát, khiến tinh trùng mất khả năng thụ tinh trước khi gặp noãn.
Trong thực hành lâm sàng, việc phân biệt chính xác giữa bạch cầu và tế bào dòng tinh là yêu cầu bắt buộc, để xác dịnh nguồn sản sinh ROS. Đồng thời, để khắc phục hạn chế của phương pháp nuôi cấy truyền thống, các nghiên cứu kiến nghị áp dụng công nghệ NGS hoặc metagenomics để đánh giá toàn diện hệ vi sinh vật trong tinh dịch.
Đối với kỹ thuật hỗ trợ sinh sản, việc sử dụng tinh trùng nhiễm khuẩn (đặc biệt là nhiễm E. coli) cho ICSI làm tăng rủi ro thất bại thụ tinh, phôi ngừng phát triển và sảy thai sớm do độc tố vi khuẩn hoặc sự lây nhiễm vào môi trường nuôi cấy. Do đó, cần ưu tiên điều trị dứt điểm tình trạng nhiễm khuẩn và cân bằng lại hệ vi sinh vật trước khi tiến hành các thủ thuật để đảm bảo chất lượng phôi và kết cục thai kỳ tốt nhất.
Tài liệu tham khảo
[1] Tvrdá E, Lovíšek D, Gálová E, Schwarzová M, Kováčiková E, Kunová S, Žiarovská J, Kačániová M. Possible Implications of Bacteriospermia on the Sperm Quality, Oxidative Characteristics, and Seminal Cytokine Network in Normozoospermic Men. Int J Mol Sci. 2022 Aug 4;23(15):8678. doi: 10.3390/ijms23158678. PMID: 35955814; PMCID: PMC9369207.
[2] Henkel R. Leukocytospermia and/or Bacteriospermia: Impact on Male Infertility. J Clin Med. 2024;13(10):2841. Published 2024 May 11. doi:10.3390/jcm13102841
[3] Fraczek M, Kurpisz M. Mechanisms of the harmful effects of bacterial semen infection on ejaculated human spermatozoa: potential inflammatory markers in semen. Folia Histochem Cytobiol. 2015;53(3):201-217. doi:10.5603/fhc.a2015.0019
[4] Neto FTL, Viana MC, Cariati F, Conforti A, Alviggi C, Esteves SC. Effect of environmental factors on seminal microbiome and impact on sperm quality. Front Endocrinol (Lausanne). 2024;15:1348186. Published 2024 Feb 22. doi:10.3389/fendo.2024.1348186
[5] Chatzokou D, Tsarna E, Davouti E, Siristatidis CS, Christopoulou S, Spanakis N, Tsakris A, Christopoulos P. Semen Microbiome, Male Infertility, and Reproductive Health. International Journal of Molecular Sciences. 2025; 26(4):1446. https://doi.org/10.3390/ijms26041446.
[6] Hofman J, Brenerova P, Borilova Linhartova P. State-of-the-art approaches in the investigation of human seminal bacteriome using metagenomic methods. Front Reprod Health. 2025;7:1557912. Published 2025 Jun 5. doi:10.3389/frph.2025.1557912.
[7] Lakhe G, Nair N, Pareek C, Ugemuge S. Bacteriospermia-Related Male Infertility: A Case Report on Diagnostic and Therapeutic Approaches. Cureus. 2024;16(6):e62973. Published 2024 Jun 23. doi:10.7759/cureus.62973.
[8] Tvrdá E, Ďuračka M, Benko F, Lukáč N. Bacteriospermia - A formidable player in male subfertility. Open Life Sci. 2022;17(1):1001-1029. Published 2022 Aug 17. doi:10.1515/biol-2022-0097
[9] Eini F, Kutenaei MA, Zareei F, Dastjerdi ZS, Shirzeyli MH, Salehi E. Effect of bacterial infection on sperm quality and DNA fragmentation in subfertile men with Leukocytospermia. BMC Mol Cell Biol. 2021;22(1):42. Published 2021 Aug 13. doi:10.1186/s12860-021-00380-8.
[10] Samantaray, Satyanarayan & Jal, Soumya & Purohit, Gopal & Chhotaray, Sangeeta. (2025). The Impact of Bacteriospermia on Sperm Survival and DNA Fragmentation in Subfertile Men. Asian Journal of Research in Pharmaceutical Sciences. 322-328. 10.52711/2231-5659.2025.00047.
[11] Azoulay Y, Malik Z, Breitbart H. Sperm interaction with bacteria induces the spontaneous acrosome reaction. Theriogenology. 2023;203:82-88. doi:10.1016/j.theriogenology.2023.02.029 .
[12] He, Y., Mao, Y., Chen, Y., Tang, L., Hou, H., Sun, C., … Li, L. (2024). Effects of Embryo Microbial Contamination on ART and Neonatal Outcomes. Infection and Drug Resistance, 17, 4137–4148. https://doi.org/10.2147/IDR.S478594.
[13] Tesarik J, Greco E, Mendoza C. Late, but not early, paternal effect on human embryo development is related to sperm DNA fragmentation. Hum Reprod. 2004;19(3):611-615. doi:10.1093/humrep/deh127.
[14] Vajpeyee, M., Tiwari, S. & Yadav, L.B. Characterization of seminal microbiome associated with semen parameters using next-generation sequencing. Middle East Fertil Soc J 29, 22 (2024). https://doi.org/10.1186/s43043-024-00181-x.