NHS. Lê Thị Mỹ Trinh, ThS. BS. Vũ Đức Công
Bệnh viện Mỹ Đức
MỞ ĐẦU
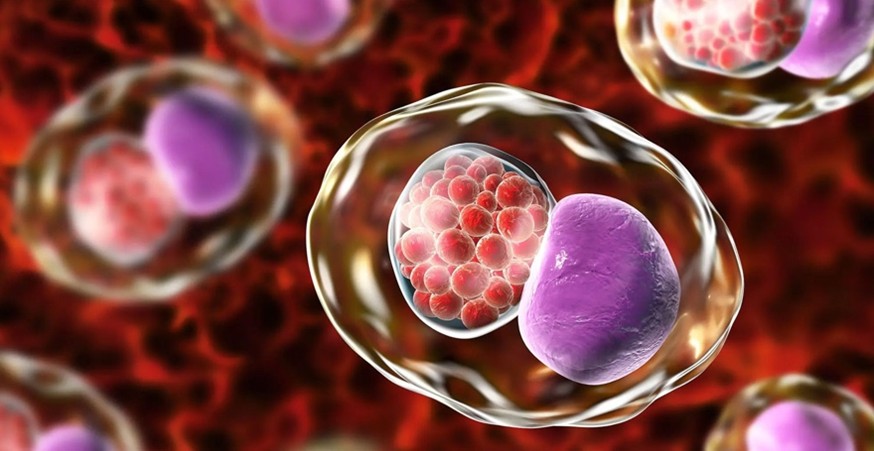
Nhiễm khuẩn đường sinh dục nam (Male Genital Tract Infection – MGTI) là nguyên nhân phổ biến thứ ba gây vô sinh nam sau giãn tĩnh mạch thừng tinh, chiếm khoảng 15% các trường hợp lâm sàng1. Điều đáng lo ngại nhất là tính thầm lặng của bệnh ở những trường hợp nhiễm khuẩn, một trong những tác nhân phổ biến là Chlamydia trachomatis (CT)2, chúng thường không biểu hiện triệu chứng lâm sàng rõ rệt do đó thường dẫn đến sự chậm trễ trong việc chẩn đoán và điều trị. Dù không gây đau đớn, những tác nhân này âm thầm kích hoạt sự huy động bạch cầu, tạo ra các gốc tự do (Reactive Oxygen Species – ROS) gây stress oxy hoá, quá trình này ảnh hưởng tiêu cực đến tinh trùng 2–5. Ngoài ra, nhiễm CT không triệu chứng còn là mối đe doạ đến bạn đời qua đường tình dục, việc lây nhiễm thầm lặng các tác nhân này dẫn đến các biến chứng phụ khoa ở phụ nữ như viêm vùng chậu (Pelvic Inflammatory Disease – PID), tắc ống dẫn trứng, tăng nguy cơ sẩy thai và các biến chứng thai kỳ nghiêm trọng2,3,6. Do đó, việc chủ động tầm soát và nhận diện tác động của nhiễm trùng đường sinh dục ngay cả khi cơ thể hoàn toàn khoẻ mạnh là bước tiên quyết để bảo vệ sức khoẻ sinh sản bền vững.
TỔNG QUAN VỀ CHLAMYDIA TRACHOMATIS
Theo Tổ chức y tế thế giới, CT là một trong các tác nhân phổ biến lây nhiễm qua đường tình dục (Sexually Transmitted Infections - STIs) phổ biến trên toàn cầu với gần 130 triệu ca mắc vào năm 20207. Vi khuẩn lây lan chủ yếu qua tiếp xúc trực tiếp với niêm mạc trong quá trình quan hệ tình dục (bao gồm cả đường âm đạo, hậu môn và miệng). Ngoài ra, vi khuẩn cũng có thể lây truyền dọc từ mẹ sang con trong quá trình sinh thường qua đường âm đạo. Đặc điểm quan trọng nhất của nhiễm Chlamydia là đa số các trường hợp mắc phải thường không có triệu chứng do đó người bệnh không nhận biết mình bị nhiễm, khiến tác nhân này dễ dàng lây lan một cách âm thầm trong cộng đồng. Tỷ lệ mắc CT được phát hiện thấy chủ yếu ở người trẻ tuổi, nhất là những trường hợp quan hệ tình dục không an toàn hoặc có nhiều bạn tình. Ở nam và nữ giới tỷ lệ không triệu chứng khi nhiễm rất cao lần lượt là 50% và khoảng 70%. Điều này cho thấy nhiễm CT là một vấn đề sức khoẻ cộng đồng đáng chú ý và cần được quan tâm2,8.
ẢNH HƯỞNG CỦA CHLAMYDIA TRACHOMATIS LÊN TINH TRÙNG
Hiện nay, mặc dù ảnh hưởng cụ thể của CT lên chất lượng tinh trùng còn nhiều tranh cãi khác nhau, các bằng chứng tổng hợp gần đây đã phân tích rõ mối nguy cơ của tác nhân này. Một phân tích gộp từ 26 nghiên cứu được chọn từ năm 2000 đến 2024 cho thấy người nhiễm CT có nguy cơ vô sinh cao gấp 3,7 lần so với người không nhiễm. Đáng chú ý, khi loại bỏ yếu tố nhiễu từ tuổi thì nguy cơ này có thể lên tới 6,7 lần. Cơ chế gây hại được ghi nhận bao gồm sự phân mảnh ADN và kích hoạt caspase-3 (một dấu hiệu của tế bào đang chết chương trình) trong tinh trùng của người nhiễm CT9. Tuy nhiên, biểu hiện trên tinh dịch đồ có thể thay đổi theo từng nghiên cứu. Theo tác giả Zhou và cộng sự, nhiễm CT có mối liên quan đáng kể với việc giảm thể tích tinh dịch (hypospermia) và tăng số lượng bạch cầu hạt đa nhân trong tinh tương (biểu hiện của phản ứng viêm), nhưng chưa ghi nhận tác động tiêu cực lên khả năng sống hay hình thái của tinh trùng10. Ngược lại, một nghiên cứu khác tại Morocco lại cho thấy sự sụt giảm có ý nghĩa thống kê (p<0,05) về cả mật độ, độ di động và hình thái tinh trùng ở nhóm nhiễm bệnh. Điểm đặc biệt là ngay cả ở nhóm nhiễm CT không triệu chứng có tinh dịch đồ đại thể bình thường, độ di động vẫn thấp hơn rõ rệt so với nhóm không nhiễm CT (59,82% so với 71,38%). Đồng thời, các tổn thương ở cấp độ phân tử như chỉ số phân mảnh ADN tinh trùng (DNA Fragmentation Index - DFI) và chỉ số tháo xoắn nhiễm sắc thể chất (Decondensation of Chromatin Index - SDI) tăng cao đáng kể (p<0,01) ở nhóm nhiễm CT, cho thấy những tác động thầm lặng mà các xét nghiệm thường quy dễ bỏ sót11.
Viêm và phản ứng stress oxy hoá
Khi xâm nhập vào đường sinh dục nam, CT kích hoạt hệ thống miễn dịch, tạo ra một môi trường độc hại cho tinh trùng thay vì môi trường nuôi dưỡng thông thường. CT kích hoạt các tế bào biểu mô tiết ra các cytokine gây viêm (như IL-1, IL-6, IL-8 và TNFa). Các tín hiệu này thu hút một lượng lớn bạch cầu (đặc biệt là bạch cầu trung tính và đại thực bào đến vị trí nhiễm trùng6. Các cytokine gây viêm không chỉ tiêu diệt vi khuẩn mà còn gây tổn thương mô. Ví dụ, TNFa và IL-6 có thể làm gián đoạn quá trình sinh tinh và phá vỡ hàng rào máu-tinh hoàn12. Phản ứng viêm mãn tính có thể gây sẹo hoá hoặc phù nề, dẫn đến tắc nghẽn ống phóng tinh. Điều này giải thích tại sao nam giới nhiễm CT thường có thể tích tinh dịch thấp bất thường (hypospermia)10.
Phản ứng viêm chính là nguồn gốc gây ra stress oxy hoá, các bạch cầu được huy động để chống lại nhiễm trùng sẽ giải phóng một lượng lớn các gốc oxy hoá tự do (Reactive Oxygen Species – ROS) như anion superoxide (O2-) và hydrogen peroxide (H2O2). Ngoài ra, chính các độc tố của vi khuẩn như lipopolysaccharide – LPS) cũng kích thích sản sinh ROS quá mức. Khi lượng ROS sinh ra vượt quá khả năng trung hoà của các chất chống oxy hoá trong tinh dịch như catalase, glutathione thì trạng thái stress oxy hoá sẽ xảy ra. Stress oxy hoá sẽ tấn công tinh trùng qua 3 mũi nhọn chính là màng tế bào, ADN và ty thể12.
Bảng 1: Tác động đa cấp độ của stress oxy hoá lên cấu trúc và chức năng của tinh trùng12
|
Cấu trúc tế bào bị ảnh hưởng |
Thành phần phân tử đích |
Cơ chế gây tổn thương |
Hậu quả lên chức năng sinh sản |
|
Màng tế bào |
Axit béo khôngbão hoà đa (Polyunsaturated Fatty Acids – PUFAs) |
Các gốc tự do (ROS) oxy hoá lớp lipid trên màng (peroxy hoá lipid) tạo ra các sản phẩm độc hại như Malondialdehyde (MDA) làm màng trở nên xơ cứng |
Tinh trùng mất khả năng di động, cản trở phản ứng cực đầu. Độ linh động màng giảm ngăn cản tinh trùng tiếp cận trứng thông qua phản ứng acrosome. |
|
Vật liệu di truyền |
ADN nhân và ADN ty thể |
ROS gây ra các đứt gãy sợi đơn và sợi đôi trong chuỗi DNA, dẫn đến biến đổi cấu trúc gen |
Tăng phân mảnh ADN tinh trùng, tăng nguy cơ sẩy thai sớm, thai lưu hoặc dị tật bẩm sinh ở thai. |
|
Cổ tinh trùng |
Ty thể |
ROS phá huỷ màng ty thể, cắt đứt nguồn cung cấp năng lượng |
Cạn kiệt năng lượng ATP, tinh trùng bất động hoặc tiến tới chậm. Suy yếu quá trình phân hoá tế bào mầm và phá vỡ quá trình sinh tinh, dẫn đến ảnh hưởng quá trình trưởng thành của tinh trùng |
Kháng thể kháng tinh trùng (Antisperm Antibodies – ASA)
Thông thường, tinh trùng được bảo vệ bởi hàng rào máu – tinh hoàn. Nhiễm trùng Chlamydia có thể phá vỡ hàng rào này hoặc kích thích miễn dịch nhận diện tinh trùng là vật thể lạ. Cơ thể sản sinh ra ASA làm tinh trùng kết dính lại với nhau gây ngưng kết, cản trở tinh trùng di chuyển qua chất nhầy cổ tử cung của người phụ nữ và ngăn cản tinh trùng thực hiện phản ứng cực đầu để xâm nhập vào trứng 6.
Giả thuyết vi khuẩn nội bào
Đây là một cơ chế xâm lấn trực tiếp biến tinh trùng thành vật chủ mang bệnh. Một vài tác giả ủng hộ giả thuyết rằng CT không chỉ bám bên ngoài mà còn xâm nhập vào bên trong đầu và cổ tinh trùng do đó trực tiếp làm hỏng cấu trúc siêu vi của tinh trùng từ bên trong. Quan trọng hơn, tinh trùng nhiễm khuẩn hoạt động như một phương tiện vận chuyển, đưa vi khuẩn vào tử cung và vòi trứng của người phụ nữ khi thụ tinh gây lây nhiễm và khó phòng ngừa cho bạn đời3.
SỨC KHOẺ PHỤ KHOA BẠN ĐỜI VÀ KẾT CỤC THAI KỲ
Sức khoẻ phụ khoa
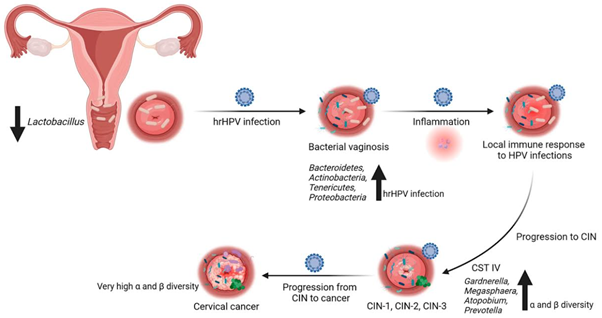
Do khoảng 50% nam giới nhiễm bệnh không có triệu chứng, họ vô tình lây truyền vi khuẩn sang bạn đời thông qua quan hệ tình dục không an toàn mà không hề hay biết 2. Thậm chí, ngay cả khi người nữ đã được điều trị khỏi, việc người nam không được chẩn đoán và điều trị song song sẽ dẫn đến tình trạng tái nhiễm liên tục, khiến vi khuẩn tồn tại dai dẳng trong đường sinh dục nữ. Ở phụ nữ, nhiễm CT không được điều trị có thể dẫn đến các hậu quả nghiêm trọng ảnh hưởng đến sức khoẻ sinh sản. Khi xâm nhập vào cơ thể nữ giới, CT thường gây nhiễm trùng ngược dòng từ cổ tử cung lên tử cung và vòi trứng3. Một trong những vấn đề đáng quan tâm là viêm vùng chậu (PID), đây là biến chứng nghiêm trọng gây viêm nhiễm lan rộng. Phản ứng miễn dịch của cơ thể với nhiễm trùng dai dẳng tạo ra môi trường viêm mãn tính, dẫn đến tổn thương mô, sẹo hoá và xơ hoá vòi trứng. Các vết sẹo làm tắc nghẽn vòi trứng và ngăn cản trứng gặp tinh trùng. Ngoài ra nhiễm CT còn gây đau vùng chậu mãn tính và viêm cổ tử cung, viêm nội mạc tử cung3,6.
Kết cục thai kỳ
Nếu thụ thai thành công trong khi đang nhiễm hoặc đã từng nhiễm CT, thai kỳ phải đối mặt với một số rủi ro. Do vòi trứng bị sẹo hoá, phôi thai bị mắc kẹt lại không thể di chuyển vào tử cung, vì thế thai ngoài tử cung có thể liên quan đến việc do nhiễm CT. Nhiễm CT gây hiện tượng nhiễm trùng làm tăng nguy cơ sẩy thai, vỡ ối sớm, sinh non, thai nhẹ cân và viêm nội mạc tử cung sau sinh. Stress oxy hoá do nhiễm trùng cũng liên quan đến việc giảm khả năng sống của phôi thai. Ngoài ra, mẹ nhiễm bệnh có thể truyền sang con khi sinh với tỷ lệ rủi ro từ 50-75%, dẫn đến viêm kết mạc mắt và viêm phổi do CT ở trẻ sơ sinh2.
ĐIỀU TRỊ VÀ QUẢN LÝ SAU ĐIỀU TRỊ
Theo hướng dẫn Châu Âu năm 2025 về quản lý nhiễm CT, các chuyên gia khuyến cáo sử dụng Doxycycline 100mg uống 2 lần/ngày trong 7 ngày là lựa chọn đầu tay thay vì Azithromycin liều duy nhất trước đây, ghi nhận cho thấy Doxycycline đạt hiệu quả diệt khuẩn lên tới >97% ở nam giới, cao hơn đáng kể so với Azithromycin. Quan trọng hơn, Doxycycline tiêu diệt triệt để vi khuẩn tại trực tràng. Nếu dùng phác đồ cũ, vi khuẩn tại trực tràng có thể sống sót và tự lây ngược lại đường sinh dục, khiến người vợ bị tái nhiễm dai dẳng và tiếp tục lây cho chồng. Việc điều trị sẽ vô nghĩa nếu chỉ thực hiện trên một người, nên hướng dẫn này quy định rõ về việc cần thông báo cho tất cả bạn tình trong 6 tháng gần nhất để họ đi xét nghiệm và điều trị. Sau khi hoàn thành điều trị, cả hai người phải kiêng quan hệ tình dục trong 7 ngày vì đây là thời gian cần thiết để thuốc tiêu diệt hoàn toàn vi khuẩn và niêm mạc phục hồi, ngăn ngừa lây nhiễm chéo ngay lập tức. Sau khi uống hết thuốc, việc quản lý vẫn chưa kết thúc, nếu tuân thủ đúng phác đồ Doxycycline thì không cần phải xét nghiệm lại ngay lập tức do hiệu quả thuốc còn cao, nhưng nên xét nghiệm lại sau 3-12 tháng vì tỷ lệ tái nhiễm thường đạt đỉnh vào khoảng 2-5 tháng sau điều trị. Việc xét nghiệm lại vào lúc này giúp phát hiện sớm các ca tái nhiễm không triệu chứng, ngăn chặn kịp thời trước khi vi khuẩn kịp gây viêm tắc vòi trứng ở nữ hoặc phá huỷ ADN tinh trùng ở nam một lần nữa2.
THÁCH THỨC TRONG SÀNG LỌC VÀ CHẨN ĐOÁN NHIỄM CHLAMYDIA
Tính thầm lặng
Nhiễm CT ghi nhận tỷ lệ không triệu chứng cao (50% ở nam và 75% ở nữ), do đó người nhiễm không thấy khó chịu và không chủ động đi khám. Điều này dẫn đến việc bệnh lây lan âm thầm trong cộng đồng và chỉ được phát hiện khi đã gây ra biến chứng như viêm vùng chậu, vô sinh hoặc ảnh hưởng đến tinh trùng 2,3,11.
Hạn chế các phương pháp xét nghiệm hiện tại
Không có phương pháp nào là hoàn hảo và sự chênh lệch giữa các phương pháp gây khó khăn cho chẩn đoán chính xác. Đầu tiên, việc dùng xét nghiệm máu ELISA thường không phân biệt được giữa nhiễm trùng đang hoạt động và nhiễm trùng trong quá khứ. ELISA là phương pháp tìm kháng thể (IgM và IgG) của cơ thể khi có vi khuẩn xâm nhập. Tuy nhiên, kháng thể chủ yếu phản ánh việc đã từng tiếp xúc chứ không khẳng định được vi khuẩn đang hoạt động. Vì cơ thể cần thời gian để sản sinh đủ kháng thể, nếu xét nghiệm quá sớm kết quả sẽ âm tính dù vi khuẩn đã bắt đầu xâm nhập. ELISA cũng có thể bỏ sót nhiều ca bệnh mà PCR phát hiện ra, cụ thể trong một nhóm nghiên cứu, ELISA chỉ phát hiện 159 ca trong khi PCR phát hiện thêm 173 ca dương tính mà ELISA cho kết quả âm tính11. PCR có thể phát hiện được ngay cả khi lượng vi khuẩn rất ít mà ELISA bỏ sót. Nếu PCR dương tính nghĩa là ADN vi khuẩn đang có mặt đồng nghĩa với việc đang bị nhiễm CT và cần điều trị ngay. Do đó, PCR được xem là tiêu chuẩn vàng của hiện tại, với độ chính xác cao nhưng chi phí cao hơn các phương pháp còn lại và đòi hỏi trang thiết bị hiện đại, khó áp dụng đại trà ở các cơ sở y tế tuyến dưới 11.
Tồn tại dai dẳng
Dưới áp lực của hệ miễn dịch hoặc thuốc kháng sinh, Chlamydia có thể chuyển sang trạng thái tồn tại dai dẳng. Lúc này, chúng biến thành các thể bất thường ngưng nhân lên nhưng vẫn sống. Ở trạng thái này, vi khuẩn không thể nuôi cấy được và có mức độ trao đổi chất rất thấp, khiến chúng dễ dàng bị bỏ sót bởi các phương tiện xét nghiệm thông thường và kháng lại các liệu pháp điều trị chuẩn6.
Biến thể vi khuẩn
Vi khuẩn CT đang biến đổi gen để trốn tránh các xét nghiệm chẩn đoán tiêu chuẩn như biến thể mất plasmid. Nhiều xét nghiệm PCR thương mại dựa vào việc tìm kiếm plasmid (một đoạn gen của vi khuẩn) để chẩn đoán. Tuy nhiên, các nhà khoa học đã phát hiện các biến thể mới như biến thể Thuỵ Điển hoặc biến thể mới tại Phần Lan đã xoá bỏ đoạn gen mục tiêu này hoặc toàn bộ plasmid dẫn đến kết quả xét nghiệm là âm tính giả dù bệnh nhân thực sự đang nhiễm bệnh. Điều này đặt ra thách thức phải phát triển các bộ kit xét nghiệm đa mục tiêu tìm cả gen trên nhiễm sắc thể của vi khuẩn chứ không chỉ plasmid3.
Quản lý nhiễm CT trong bối cảnh hiếm muộn và hỗ trợ sinh sản
Trong thực hành tại các cơ sở hỗ trợ sinh sản, tầm soát và xử trí CT nên được lồng ghép vào quy trình đánh giá cặp vợ chồng hiếm muộn, đặc biệt ở các trường hợp có yếu tố nguy cơ hành vi, tiền sử viêm vùng chậu, bất thường ống dẫn trứng hoặc tinh dịch đồ gợi ý viêm. Khi phát hiện một trong hai vợ chồng dương tính với CT, cần điều trị đồng thời cả hai, trì hoãn các kỹ thuật hỗ trợ sinh sản cho đến khi hoàn tất phác đồ và nếu có thể, đạt kết quả xét nghiệm âm tính, nhằm giảm nguy cơ biến chứng phụ khoa và thai kỳ.
Đối với các phác đồ hỗ trợ sinh sản có sử dụng tinh trùng (IUI, IVF, ICSI), bác sĩ nam khoa và bác sĩ điều trị hiếm muộn cần phối hợp chặt chẽ để đánh giá nguy cơ nhiễm trùng, lựa chọn thời điểm can thiệp tối ưu và tư vấn cho cặp vợ chồng về lợi ích của việc điều trị triệt để CT trước khi tiến hành các thủ thuật xâm lấn.
KẾT LUẬN
Nhiễm CT ở nam giới không chỉ đơn thuần là một bệnh lý nhiễm trùng đường sinh dục, mà thực sự là một tác nhân thầm lặng đe doạ trực tiếp đến tiềm năng sinh sản của cả cặp đôi. Các bằng chứng hiện tại đã cho thấy CT không chỉ tác động ở phản ứng viêm cục bộ mà còn đi sâu vào cấp độ phân tử thông qua stress oxy hoá và sự gia tăng phân mảnh ADN tinh trùng, ngay cả khi các chỉ số tinh dịch đồ cơ bản vẫn nằm trong giới hạn bình thường. Quan trọng hơn, vai trò của nam giới như một nguồn lây nhiễm tiềm ẩn có thể dẫn đến những hệ luỵ cho sức khoẻ phụ khoa của người bạn đời và kết cục thai kỳ như sẩy thai và sinh non. Do đó, việc thay đổi quan điểm lâm sàng từ điều trị khi có triệu chứng sang chủ động sàng lọc thường quy là hết sức cần thiết.
TÀI LIỆU THAM KHẢO
1. Rivero MJ, Kulkarni N, Thirumavalavan N, Ramasamy R. Evaluation and Management of Male Genital Tract Infections in the Setting of Male Infertility: An Updated Review. Curr Opin Urol. 2023;33(3):180-186. doi:10.1097/MOU.0000000000001081
2. White JA, Dukers-Muijrers NH, Hoebe CJ, Kenyon CR, Dc Ross J, Unemo M. 2025 European guideline on the management of Chlamydia trachomatis infections. Int J STD AIDS. 2025;36(6):434-449. doi:10.1177/09564624251323678
3. Rodrigues R, Sousa C, Barros A, Vale N. Chlamydia trachomatis: From Urogenital Infections to the Pathway of Infertility. Genes. 2025;16(2):205. doi:10.3390/genes16020205
4. Guiton R, Drevet JR. Viruses, bacteria and parasites: infection of the male genital tract and fertility. Basic Clin Androl. 2023;33:19. doi:10.1186/s12610-023-00193-z
5. Wang Y, Fu X, Li H. Mechanisms of oxidative stress-induced sperm dysfunction. Front Endocrinol. 2025;16. doi:10.3389/fendo.2025.1520835
6. Redgrove KA, McLaughlin EA. The Role of the Immune Response in Chlamydia trachomatis Infection of the Male Genital Tract: A Double-Edged Sword. Front Immunol. 2014;5:534. doi:10.3389/fimmu.2014.00534
7. Sexually transmitted infections (STIs). Accessed February 11, 2026. https://www.who.int/news-room/fact-sheets/detail/sexually-transmitted-infections-(stis)
8. INTRODUCTION. In: WHO Guidelines for the Treatment of Chlamydia Trachomatis. World Health Organization; 2016. Accessed January 20, 2026. https://www.ncbi.nlm.nih.gov/books/NBK379712/
9. Bragazzi NL, Bosch Castells V, Deng Q, et al. The Impact of Chlamydia trachomatis on Male Infertility: A Systematic Review and Meta-Analysis. Open Forum Infect Dis. 2025;13(1):ofaf782. doi:10.1093/ofid/ofaf782
10. Zhou H, Wu S, Tang X, et al. Chlamydia trachomatis infection in the genital tract is associated with inflammation and hypospermia in the infertile male of China. Asian J Androl. 2022;24(1):56. doi:10.4103/aja.aja_54_21
11. Kabbour M, Mbaye MM, Ghazi B, et al. Molecular Characterization of Chlamydia trachomatis Infection and Its Impact on Sperm Characteristics of Moroccan Infertile Men. Infect Dis Rep. 2025;17(6):135. doi:10.3390/idr17060135
12. Potiris A, Moustakli E, Trismpioti E, et al. From Inflammation to Infertility: How Oxidative Stress and Infections Disrupt Male Reproductive Health. Metabolites. 2025;15(4):267. doi:10.3390/metabo15040267