CNSH. Lê Thị Quỳnh, ThS. Trương Thị Thanh Bình, ThS. BS. Dương Công Bằng
Bệnh viện Phụ sản Quốc tế Sài Gòn
-
Mở đầu
Bệnh quai bị, do virus quai bị (Mumps virus - MuV) thuộc họ Paramyxoviridae gây ra, đang là một trong những thách thức lớn trong lĩnh vực nam học và y học sinh sản hiện đại. Mặc dù sự ra đời của vaccine sởi - quai bị - rubella (MMR - Measles, Mumps, Rubella) đã làm giảm tỷ lệ mắc bệnh trên toàn cầu lên đến 99% tại một số khu vực, tuy nhiên sự bùng phát bệnh vẫn tiếp tục xảy ra tại nhiều quốc gia[1]. Theo dữ liệu từ Tổ chức Y tế Thế giới (World Health Organization - WHO), số ca mắc quai bị toàn cầu năm 2023 đạt gần 400.000 ca, tăng nhẹ so với năm trước đó. Điều này cho thấy MuV vẫn là một vấn đề y tế đáng được quan tâm[1].
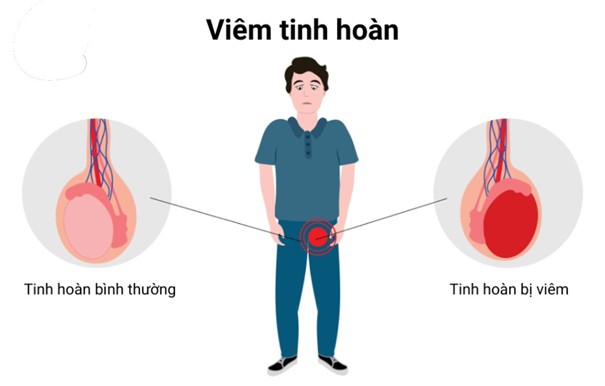
Di chứng nghiêm trọng nhất đối với nam giới là viêm tinh hoàn, thường xuất hiện sau tình trạng viêm tuyến mang tai. Tỷ lệ nam giới sau dậy thì gặp di chứng này dao động từ 15% - 40%, tập trung nhiều ở nhóm tuổi từ 15 - 24 tuổi[2]. Khoảng 10% - 30% các trường hợp xảy ra ở cả hai bên tinh hoàn và nhóm bệnh nhân này có nguy cơ vô sinh, suy tuyến sinh dục do teo tinh hoàn diễn tiến nhanh sau giai đoạn viêm cấp[2].
-
Quá trình xâm nhập của virus và những biến đổi miễn dịch bất thường tại tinh hoàn
Virus quai bị có đặc tính hướng mô với các tế bào trong biểu mô sinh tinh. MuV sử dụng protein hemagglutinin-neuraminidase (HN) để gắn kết với các thụ thể chứa acid sialic trên bề mặt tế bào vật chủ[2], xâm nhập vào khoang kẽ và tấn công các tế bào Leydig, gây gián đoạn quá trình sinh tổng hợp testosterone thông qua ức chế enzyme CYP17A1[3]. Sự sụt giảm testosterone không chỉ ảnh hưởng đến chức năng nội tiết mà còn làm mất đi tín hiệu cần thiết để duy trì quá trình sinh tinh bình thường. Khi xâm nhập sâu vào các ống sinh tinh, MuV tấn công tế bào Sertoli – thành phần chính của hàng rào máu - tinh hoàn (BTB – Blood-Testis Barrier)[3].
Đáp ứng miễn dịch được kích hoạt ngay lập tức sau khi nhiễm virus. MuV kích thích các tế bào Sertoli giải phóng một lượng lớn các cytokine tiền viêm như TNF-α, IL-6 và IL-1β chỉ trong vòng 4 giờ đầu[4]. Nồng độ TNF-α tăng cao đột ngột làm phân rã các protein liên kết quan trọng, dẫn đến phá vỡ cấu trúc nguyên vẹn của BTB[3]. Sự phá vỡ này đã cho phép hệ thống miễn dịch của cơ thể tiếp xúc với các kháng nguyên tinh trùng, kích hoạt phản ứng miễn dịch tự miễn và tạo ra kháng thể kháng tinh trùng. Quá trình này làm tình trạng suy giảm khả năng sinh sản trở nên nghiêm trọng hơn[5]. Các nghiên cứu mới nhất của Gan và cộng sự (2025) và Li và cộng sự (2025) còn chỉ ra rằng MuV thúc đẩy quá trình pyroptosis – một dạng chết tế bào do viêm thông qua sự hoạt hóa của inflammasome NLRP3 và protein Gasdermin D, dẫn đến sự sụt giảm hàng loạt tế bào mầm sinh tinh và tế bào Sertoli[6,7].
-
Hội chứng chèn ép khoang tinh hoàn và di chứng teo tinh hoàn
Viêm tinh hoàn do quai bị thường khởi phát sau khi viêm tuyến mang tai khoảng một tuần[2]. Bệnh nhân thường xuất hiện các triệu chứng toàn thân như sốt cao (có thể lên tới 40°C), rét run, đau đầu và buồn nôn[2]. Tại vùng bìu, tinh hoàn bị ảnh hưởng (thường là một bên) sưng to gấp 2-3 lần bình thường, gây đau đớn dữ dội lan xuống vùng bẹn. Da bìu trở nên căng, đỏ, nóng và phù nề[2].
Tinh hoàn được bao bọc bởi lớp vỏ bao trắng (tunica albuginea), đây là một màng xơ dày và hầu như không có tính đàn hồi[8]. Khi hiện tượng phù nề nhu mô và thâm nhiễm tế bào diễn ra mạnh mẽ, áp lực bên trong tinh hoàn tăng lên nhanh chóng. Do lớp vỏ bao trắng không thể giãn nở để giải tỏa áp lực này nên các vi mao mạch cung cấp oxy và dinh dưỡng cho các ống sinh tinh bị chèn ép nghiêm trọng[8]. Khi áp lực nội mô này vượt quá áp lực trong lòng mao mạch (thường trên 30 mmHg), sẽ gây ra "Hội chứng chèn ép khoang tinh hoàn" (Testicular Compartment Syndrome - TCS)[8].
Sự gia tăng áp lực bên trong tinh hoàn dẫn đến thiếu máu cục bộ, nhồi máu nhu mô và hoại tử biểu mô sinh tinh[8]. Đây là nguyên nhân cơ bản dẫn đến tình trạng teo tinh hoàn, được ghi nhận ở 30% - 50% bệnh nhân sau khi đợt viêm cấp tính kết thúc[9]. Di chứng teo tinh hoàn diễn ra âm thầm trong vòng 25 - 230 ngày sau khi mắc bệnh, dẫn đến sự suy giảm thể tích và mất đi độ đàn hồi bình thường của tinh hoàn[10].
Bảng 1: So sánh đặc điểm tinh hoàn bình thường và tinh hoàn sau viêm quai bị
|
Đặc điểm so sánh |
Tinh hoàn bình thường |
Tinh hoàn sau viêm quai bị (giai đoạn bị teo) |
TLTK |
|
Thể tích trung bình |
15 – 25mL |
Giảm 20% - 55% thể tích |
Choi và cộng sự (2020)[11] |
|
Hình thái trên siêu âm |
Hình trứng, đồng nhất |
Hình thuôn dài, không đồng nhất |
Wu và cộng sự (2021)[2] |
|
Tình trạng tưới máu (siêu âm Doppler) |
Bình thường |
Giảm tưới máu rõ rệt |
Wu và cộng sự (2021)[2] |
|
Cấu trúc ống sinh tinh |
Đầy đặn, hoạt động sinh tinh diễn ra bình thường |
Xơ hoá, hyalin hoá |
Choi và cộng sự (2020)[11] |
-
Tác động của bệnh quai bị đến các thông số tinh dịch đồ và khả năng sinh sản của nam giới
Mặc dù các triệu chứng của quai bị chỉ kéo dài trong vòng 7-10 ngày, nhưng những di chứng đối với khả năng sinh sản của nam giới có thể kéo dài suốt đời[12].
Viêm tinh hoàn do quai bị hiếm khi dẫn đến vô sinh hoàn toàn nếu chỉ bị một bên, nhưng nó thường gây ra tình trạng thiểu tinh[8]. Mật độ tinh trùng có thể giảm xuống mức rất thấp, độ di động bị hạn chế và tỷ lệ hình dạng bất thường tăng cao do quá trình sinh tinh bị ảnh hưởng nghiêm trọng[8]. Trong trường hợp viêm tinh hoàn hai bên, nguy cơ azoospermia (không có tinh trùng trong tinh dịch) là rất cao, với tỷ lệ mắc khoảng 30% - 87% trường hợp[8]. Ngay cả khi mật độ tinh trùng phục hồi sau giai đoạn cấp tính, chất lượng DNA của tinh trùng thường vẫn bị tổn thương do hậu quả của quá trình viêm và stress oxy hóa kéo dài[13].
Sự tổn thương tế bào Leydig trong giai đoạn viêm cấp tính có thể dẫn đến tình trạng suy sinh dục một phần hoặc hoàn toàn[2]. Mặc dù nồng độ testosterone cơ bản có thể trở lại giới hạn bình thường sau 6-12 tháng ở nhiều bệnh nhân, nhưng nồng độ FSH và LH vẫn thường duy trì ở mức cao hơn so với người khỏe mạnh[8]. Điều này cho thấy trục hạ đồi - tuyến yên - tinh hoàn phải hoạt động ở mức tối đa để duy trì nồng độ nội tiết tố, và từ đó phản ánh tình trạng suy tinh hoàn tiềm ẩn trong tương lai[8].
Theo số liệu thống kê, khoảng 23,5% nam giới từng bị viêm tinh hoàn do quai bị có sự xuất hiện của các kháng thể kháng tinh trùng trong tinh dịch. Các kháng thể này bám vào bề mặt tinh trùng, làm giảm khả năng di động và ngăn cản quá trình thụ tinh với noãn[14]. Sự hiện diện của kháng thể kháng tinh trùng là một trong những cơ chế giải thích tại sao một số nam giới vẫn vô sinh mặc dù các thông số tinh dịch đồ cơ bản có vẻ bình thường[15].
-
Chiến lược giảm thiểu tác động của quai bị lên khả năng sinh sản
5.1. Chẩn đoán
Chẩn đoán sớm sẽ giúp điều trị và theo dõi sớm, hạn chế các di chứng. Chẩn đoán viêm tinh hoàn do quai bị chủ yếu dựa trên khai thác tiền sử bệnh lý và thăm khám thực thể, vì các dấu hiệu của bệnh khá điển hình. Bác sĩ sẽ xác định tiền sử sưng tuyến mang tai, đi kèm với các triệu chứng đau và sưng tấy tại tinh hoàn[2]. Kích thước và thể tích tinh hoàn được đánh giá bằng thước đo Prader[2].
Siêu âm Doppler màu là phương pháp chẩn đoán đầu tay. Hình ảnh Doppler cho phép quan sát chi tiết mức độ viêm trong giai đoạn cấp thông qua các dấu hiệu tăng tưới máu và phù nề nhu mô, giúp xác định mức độ nghiêm trọng của bệnh[11].
Xét nghiệm huyết thanh giúp xác nhận sự hiện diện của virus ở giai đoạn cấp tính thông qua kháng thể IgM đặc hiệu[8]. Cuối cùng, để đánh giá tác động tới khả năng sinh sản, xét nghiệm tinh dịch đồ cần được thực hiện ít nhất từ 3 đến 6 tháng, sau khi bệnh nhân đã phục hồi hoàn toàn. Khoảng thời gian này tương ứng với một chu kỳ sinh tinh mới, giúp đưa ra những số liệu khách quan nhất về tác động lâu dài của virus đối với chất lượng và mật độ tinh trùng[2].
5.2. Dự phòng và điều trị quai bị giai đoạn cấp
Tiêm phòng vaccine MMR là biện pháp hiệu quả nhất để ngăn ngừa bệnh quai bị và các biến chứng sau đó[9]. Trong giai đoạn viêm cấp tính, mặc dù chưa có thuốc điều trị đặc hiệu MuV, các biện pháp hỗ trợ như nghỉ ngơi tại giường, cố định bìu, chườm lạnh và sử dụng thuốc kháng viêm không steroid giúp giảm đau và giảm áp lực bên trong tinh hoàn[8].
Một số thử nghiệm lâm sàng quy mô nhỏ ghi nhận Interferon có thể làm giảm tỷ lệ teo tinh hoàn và vô tinh thông qua việc ức chế sự nhân bản của virus. Tuy nhiên, các các nghiên cứu với cỡ mẫu lớn hơn lại cho thấy hiệu quả của phương pháp này không hoàn toàn đồng nhất và không phải bệnh nhân nào cũng đạt được sự phục hồi chức năng sinh sản hoàn toàn[8]. Chính vì vậy, Interferon hiện vẫn chưa được đưa vào các hướng dẫn điều trị thường quy.
-
Điều trị vô sinh nam do quai bị trong hỗ trợ sinh sản
Điều trị vô sinh nam sau quai bị đã chuyển hướng từ phục hồi sinh tinh sang các kỹ thuật tìm kiếm và sử dụng tinh trùng còn sót lại thông qua hỗ trợ sinh sản (HTSS)[16]. Đây là mảnh ghép mới và rất quan trọng trong quản lý bệnh nhân đã mắc quai bị.
6.1. Bảo tồn khả năng sinh sản thông qua trữ lạnh tinh trùng
Đối với nam giới mắc quai bị sau tuổi dậy thì, việc trữ lạnh tinh trùng ngay trong giai đoạn sớm của bệnh hoặc ngay sau khi các triệu chứng cấp tính thuyên giảm là một chiến lược bảo tồn khả năng sinh sản tối ưu[16]. Do tổn thương tinh hoàn có thể tiến triển âm thầm dẫn đến azoospermia sau vài tháng, việc lưu trữ mẫu tinh dịch ngay khi còn tinh trùng giúp tránh được các phẫu thuật xâm lấn sau này[13]. Ngay cả khi mẫu tinh trùng có chất lượng thấp như thiểu tinh, phương pháp tiêm tinh trùng vào bào tương noãn (Intra-Cytoplasmic Sperm Injection – ICSI) hiện nay vẫn có hiệu quả để tạo phôi[13].
6.2. Ứng dụng vi phẫu thuật micro-TESE trong điều trị vô sinh sau quai bị
Đối với những bệnh nhân đã tiến triển đến vô sinh không do tắc (Non-Obstructive Azoospermia - NOA) với tinh hoàn teo và không có tinh trùng trong tinh dịch, phẫu thuật vi phẫu tìm tinh trùng từ tinh hoàn (micro-TESE) là phương pháp cuối cùng ở thời điểm hiện tại[16].
Sau khi bị viêm do quai bị, cấu trúc tinh hoàn của bệnh nhân thường chuyển sang trạng thái xơ hóa, khiến phần lớn nhu mô bị tổn thương. Tuy nhiên, sâu trong các mô xơ này vẫn có thể tồn tại các vùng sinh tinh khu trú (focal spermatogenesis), nơi tinh trùng vẫn được sản xuất ở quy mô nhỏ[16]. Do tính chất phân bố không đều này, các kỹ thuật chọc hút bằng kim thông thường như TESA hay PESA thường không mang lại kết quả bởi vị trí lấy mẫu trên tinh hoàn được chọn lựa ngẫu nhiên, dẫn đến dễ bỏ lỡ các vị trí còn sinh tinh[17].
Để khắc phục hạn chế đó, kỹ thuật micro-TESE được xem là “tiêu chuẩn vàng”, nhờ khả năng can thiệp chính xác dưới kính hiển vi phẫu thuật có độ phóng đại từ 15 - 25 lần[16]. Phẫu thuật viên có thể quan sát trực tiếp và toàn diện nhu mô tinh hoàn để nhận diện các ống sinh tinh tiềm năng. Những ống này thường có kích thước lớn hơn, màu trắng đục và trông đầy đặn hơn so với các vùng xơ xung quanh, vốn là những dấu hiệu đặc trưng của vùng vẫn còn hoạt động sinh tinh[16].
Micro-TESE không chỉ nâng cao tỷ lệ tìm thấy tinh trùng mà còn đóng vai trò quan trọng trong việc bảo tồn chức năng sản xuất nội tiết nam của tinh hoàn. Bằng cách tập trung lấy đúng mẫu tại vùng nghi ngờ và giảm thiểu tối đa việc cắt bỏ nhu mô thừa, kỹ thuật này giúp bảo vệ các tế bào Leydig còn sót lại[16]. Sự bảo tồn này giúp duy trì nồng độ hormone testosterone, từ đó giảm thiểu nguy cơ suy sinh dục và các rối loạn chức năng sau phẫu thuật cho nam giới[16].
6.3. Tỷ lệ thu hồi tinh trùng (Sperm Retrieval Rate - SRR) và so sánh với các nguyên nhân NOA khác
Dữ liệu từ các nghiên cứu đa trung tâm và phân tích tổng hợp trên PubMed cho thấy NOA do quai bị có tiên lượng tìm thấy tinh trùng tốt nhất trong nhóm vô sinh do tổn thương tinh hoàn[18].
Bảng 2: So sánh tỷ lệ thu hồi tinh trùng thành công ở nhóm NOA do quai bị với nhóm NOA khác
|
Nguyên nhân gây NOA |
Tỷ lệ tìm thấy tinh trùng |
Đặc điểm ống sinh tinh |
TLTK |
|
Viêm tinh hoàn do quai bị |
75% – 94,4% |
Ống sinh tinh giãn nở khu trú giữa mô xơ |
Do và cộng sự (2025)[18] |
|
Tinh hoàn ẩn |
69% – 84,8% |
Teo ống sinh tinh nhưng vẫn có các vùng sinh tinh |
Gao và cộng sự (2022)[19] |
|
Vi mất đoạn AZFc |
56,5% – 71% |
Sinh tinh không đồng nhất |
Gilbert và cộng sự[16] |
|
Hội chứng Klinefelter |
42,4% – 50% |
Ống sinh tinh hyalin hoá mạnh |
Gilbert và cộng sự[16] |
|
NOA không rõ nguyên nhân |
27,6% – 36,4% |
Tổn thương toàn bộ |
Gao và cộng sự (2022)[19] |
Sự thành công cao trong nhóm quai bị được giải thích là do trước khi bị virus tấn công, tinh hoàn của bệnh nhân đã hoàn thiện chức năng sinh tinh. Virus chỉ phá hủy một phần nhu mô, để lại những vùng nguyên vẹn mà phẫu thuật vi phẫu có thể tìm thấy[19].
6.4. Hiệu quả của ICSI với tinh trùng trích xuất từ tinh hoàn
Sau khi đã thu thập được tinh trùng thông qua micro-TESE, kỹ thuật ICSI là bắt buộc để đạt được sự thụ tinh[18]. Các kết quả phôi học và lâm sàng ở nhóm bệnh nhân này cho kết quả tốt.
Các nghiên cứu so sánh trực tiếp của Pham và cộng sự (2025) và T Nguyen Phan và cộng sự (2024) đã chỉ ra rằng tinh trùng thu được từ bệnh nhân vô sinh do quai bị có sức sống và khả năng tạo phôi cao hơn so với các nhóm NOA khác[18,20]. Cụ thể, về tỷ lệ thụ tinh, nhóm bệnh nhân tiền sử quai bị đạt mức từ 66,1% đến 77,8%, cao hơn đáng kể so với mức 57,7% ở nhóm vô tinh không rõ nguyên nhân[20]. Ưu thế này tiếp tục được duy trì trong quá trình phát triển phôi, khi tỷ lệ phôi tốt ở giai đoạn phân chia (ngày 3) đạt khoảng 17,9%, cao hơn so với mức 13,3% của các nhóm NOA khác[20]. Đặc biệt, tỷ lệ phát triển thành phôi nang ở ngày 5 đạt tới 60,4%, một con số rất cao trong thụ tinh trong ống nghiệm[18]. Mặc dù quá trình viêm và xơ hóa có thể khiến số lượng tinh trùng thu được từ tinh hoàn teo cực kỳ khan hiếm, nhưng chất lượng di truyền và khả năng thụ tinh với noãn vẫn ổn định, được thể hiện ở bảng 3.
Bảng 3: Kết quả lâm sàng sau ICSI ở nhóm NOA do quai bị
|
Kết quả lâm sàng sau ICSI |
Tỷ lệ phần trăm |
TLTK |
|
Tỷ lệ thai dương tính (β-hCG+) |
80,2% – 82,8% |
Do và cộng sự (2025)[18] |
|
Tỷ lệ thai lâm sàng (có tim thai) |
85,71% |
Gao và cộng sự (2022)[19] |
|
Tỷ lệ thai diễn tiến (trên 30 tuần) |
38,5% – 69% |
Do và cộng sự (2025)[18] |
|
Tỷ lệ trẻ sinh sống |
66,67% |
Gao và cộng sự (2022)[19] |
Tuổi của người vợ ảnh hưởng đến kết cục. Các nghiên cứu chỉ ra rằng khi đã tìm thấy tinh trùng, yếu tố nam giới (nguyên nhân gây NOA) không còn là rào cản chính, mà chính chất lượng noãn và độ tuổi mẹ mới là yếu tố tiên lượng chính[19].
6.5. Một số vấn đề liên quan trong điều trị vô sinh sau quai bị
Cân nhắc lựa chọn nguồn gốc tinh trùng sử dụng cho ICSI:
Môi trường viêm nhiễm sau quai bị thường làm tăng chỉ số phân mảnh DNA tinh trùng (DNA Fragmentation Index – DFI), ảnh hưởng đến chất lượng phôi. Các nghiên cứu mới ưu tiên việc sử dụng tinh trùng lấy trực tiếp từ tinh hoàn thay vì tinh trùng trong tinh dịch. Kết qủa từ các nghiên cứu cho thấy tinh trùng từ tinh hoàn có DFI thấp hơn đáng kể, từ 25% - 30% so với tinh trùng từ tinh dịch[20]. Nguyên nhân là tinh trùng từ tinh hoàn chưa phải trải qua quá trình stress oxy hóa trong quá trình di chuyển qua mào tinh hoàn.
Áp dụng kỹ thuật vi phẫu micro-TESE kết hợp với trữ lạnh tinh trùng:
Việc đồng thời phẫu thuật micro-TESE cho người chồng và chọc hút noãn cho người vợ luôn là một thách thức lớn. Mặc dù tinh trùng tươi được ghi nhận có tỷ lệ thụ tinh và thai lâm sàng cao hơn, nhưng kết quả từ các nghiên cứu cho thấy sự khác biệt này không có ý nghĩa thống kê so với sử dụng mẫu đông lạnh. Điều này mở ra hướng tiếp cận linh hoạt hơn cho các cặp vợ chồng đang điều trị vô sinh do quai bị[18]. Ưu tiên thực hiện micro-TESE trước để trữ đông tinh trùng giúp chủ động trong quá trình điều trị. Chỉ khi tìm thấy tinh trùng từ người chồng, người vợ mới bắt đầu quá trình kích thích buồng trứng và chọc hút noãn. Chiến lược này giúp giảm đáng kể gánh nặng tâm lý cũng như rủi ro tài chính, tránh tình trạng người vợ phải trải qua các thủ thuật xâm lấn tốn kém nhưng sau đó lại không có tinh trùng để thụ tinh[18].
Tại Việt Nam, các nghiên cứu thực tiễn trong giai đoạn 2024 – 2025 đã cho thấy hiệu quả vượt trội của kỹ thuật vi phẫu micro-TESE kết hợp với trữ lạnh tinh trùng. Với nhóm bệnh nhân NOA sau quai bị, SRR đã đạt tới mức là 94,1%[18]. Kết quả này không chỉ mang lại tỷ lệ có thai lâm sàng cao mà còn giúp tối ưu phác đồ điều trị.
-
Kết luận
Viêm tinh hoàn do virus quai bị là di chứng nguy hiểm nhất đối với sức khỏe sinh sản nam giới. Mặc dù các kỹ thuật HTSS hiện đại như kỹ thuật vi phẫu micro-TESE kết hợp với ICSI đã mở ra hy vọng làm cha cho những bệnh nhân vô tinh, nhưng quy trình điều trị vẫn còn nhiều thách thức.
Chiến lược quản lý hiệu quả nhất vẫn là phòng ngừa chủ động bằng cách tiêm chủng đầy đủ hai liều vaccine MMR cho trẻ em và thanh thiếu niên. Đối với nam giới đã mắc bệnh, cần theo dõi và can thiệp nội khoa kịp thời để hạn chế tối đa mức độ teo tinh hoàn.
Tài liệu tham khảo:
[1] Agrawal, R., et al. (2025). Epidemiological trends and determinants of mumps outbreaks: a systematic review and meta-analysis. Frontiers in public health, 13, 1711759. https://doi.org/10.3389/fpubh.2025.1711759
[2] Wu, H., et al. (2021). Mumps Orchitis: Clinical Aspects and Mechanisms. Frontiers in immunology, 12, 582946. https://doi.org/10.3389/fimmu.2021.582946
[3] Wu, H., et al. (2019). Mumps virus infection disrupts blood-testis barrier through the induction of TNF-α in Sertoli cells. FASEB journal : official publication of the Federation of American Societies for Experimental Biology, 33(11), 12528–12540. https://doi.org/10.1096/fj.201901089R
[4] Franklin, L., et al. (2025). Mumps virus infection triggers early pro-inflammatory responses and impairs Leydig and Sertoli cell function in an ex vivo human testis model. Human reproduction (Oxford, England), 40(12), 2231–2246. https://doi.org/10.1093/humrep/deaf155
[5] Chandrashekar, P., et al. (2015). A rare case of mumps orchitis. Journal of pharmacy & bioallied sciences, 7(Suppl 2), S773–S775. https://doi.org/10.4103/0975-7406.163555
[6] Gan, Y. Q., et al. (2025). Impaired NLRP3 inflammasome signaling diverts pyroptotic to apoptotic caspase activation in macrophages. Frontiers in Immunology, 16, 1631152.
[7] Li, X., Zhang., et al. (2025). NLRP3 inflammasome and pyroptosis: implications in inflammation and multisystem disorders. PeerJ, 13, e19887. https://doi.org/10.7717/peerj.19887
[8] Masarani, M., et al. (2006). Mumps orchitis. Journal of the Royal Society of Medicine, 99(11), 573–575. https://doi.org/10.1177/014107680609901116
[9] Centers for Disease Control and Prevention. (2025). Chapter 9: Mumps. Manual for the surveillance of vaccine-preventable diseases. https://www.cdc.gov/surv-manual/php/table-of-contents/chapter-9-mumps.html
[10] Rausch-Phung, E. A., Davison, P., & Morris, J. (2024). Mumps. Trong StatPearls. StatPearls Publishing. https://www.ncbi.nlm.nih.gov/books/NBK534785/
[11] Choi, H. I., et al. (2020). Testicular atrophy after mumps orchitis: ultrasonographic findings. Ultrasonography (Seoul, Korea), 39(3), 266–271. https://doi.org/10.14366/usg.19097
[12] Wu, H., et al. (2021). Mumps orchitis: Clinical aspects and mechanisms. Frontiers in Immunology, 12, 582946. https://doi.org/10.3389/fimmu.2021.582946
[13] Tamburrino, L., et al. (2023). Cryopreservation of Human Spermatozoa: Functional, Molecular and Clinical Aspects. International Journal of Molecular Sciences, 24(5), 4656. https://doi.org/10.3390/ijms24054656
[14] Haratian, K., et al. (2025). Potential causes and associated conditions with anti-sperm antibody production among infertile males: a systematic literature review. BMC immunology, 26(1), 58. https://doi.org/10.1186/s12865-025-00740-5
[15] Franklin, et al. (2025). Mumps virus infection triggers early pro-inflammatory responses and impairs Leydig and Sertoli cell function in an ex vivo human testis model. Human reproduction (Oxford, England), 40(12), 2231–2246. https://doi.org/10.1093/humrep/deaf155
[16] Gilbert, B. R. (n.d.). TESE and microTESE: Patient guide to sperm retrieval, lab processing, and fertility success. Men's Reproductive Health. https://mensreproductivehealth.com/tese-and-microtese-patient-guide-to-sperm-retrieval-lab-processing-and-fertility-success/
[17] Chen, X., et al. (2019). Comparison and outcomes of nonobstructive azoospermia patients with different etiology undergoing MicroTESE and ICSI treatments. Translational Andrology and Urology,