KS. Cao Vân Anh, CN. Lê Thị Bích Liên, BS. Nguyễn Đỗ Thị Phương Thảo
Bệnh viện Đa khoa Gia đình, Đà Nẵng
1. GIỚI THIỆU
Ung thư cổ tử cung là gánh nặng sức khoẻ lớn ở phụ nữ, chủ yếu do nhiễm dai dẳng virus gây u nhú (Human papillomavirus – HPV) nguy cơ cao. Tuy nhiên, phần lớn trường hợp nhiễm HPV được đào thải tự nhiên, cho thấy tiến triển bệnh phụ thuộc không chỉ vào đặc tính của virus mà còn vào các yếu tố vật chủ. Trong bối cảnh đó, vi môi trường cổ tử cung – âm đạo đóng vai trò quan trọng thông qua việc duy trì hàng rào biểu mô, kiểm soát viêm và định hình đáp ứng miễn dịch niêm mạc. Hệ vi sinh ưu thế Lactobacillus hỗ trợ đào thải HPV hiệu quả, trong khi tình trạng loạn khuẩn làm tăng viêm và nguy cơ nhiễm kéo dài 1.
Bên cạnh vai trò đã được khẳng định trong sinh ung thư, HPV ngày càng được quan tâm vì những ảnh hưởng tiềm tàng đến sức khỏe sinh sản của phụ nữ, dù các bằng chứng hiện còn chưa thống nhất. Do đó, việc xem xét HPV trong bối cảnh tương tác virus- miễn dịch - hệ vi sinh cổ tử cung – âm đạo là cần thiết để hiểu toàn diện các hệ quả sinh học của nhiễm HPV. Trên cơ sở đó, bài viết này sẽ trình bày một cách tổng quan về vai trò của hệ vi sinh cổ tử cung – âm đạo trong điều hòa nhiễm HPV và sự tồn tại dai dẳng của virus, đồng thời đặt nền tảng cho việc đánh giá các ảnh hưởng của HPV đối với sức khoẻ sinh sản phụ nữ ở các phần tiếp theo.
-
CƠ CHẾ NHIỄM HPV VÀ NGUY CƠ UNG THƯ CỔ TỬ CUNG
Human papillomavirus (HPV) là virus DNA mạch đôi, kích thước nhỏ, không có vỏ bọc, có tính hướng biểu mô cao, đặc biệt là biểu mô lát tầng của cổ tử cung. Phân loại HPV chủ yếu dựa trên sự khác biệt trong trình tự DNA của virus, hiện được chia thành năm chi chính gồm alpha, beta, gamma, mu và nu. Trong đó, các chủng thuộc chi alpha có khả năng gây nhiễm tại đường sinh dục và được phân thành HPV nguy cơ cao (high-risk HPV, hr-HPV) và nguy cơ thấp (low-risk HPV, lr-HPV) dựa trên tiềm năng sinh ung thư. Đến nay, đã xác định ít nhất 448 chủng HPV khác nhau, trong đó khoảng 15 chủng được xếp vào nhóm có khả năng sinh ung thư. Nổi bật nhất HPV16 và HPV18, hai chủng liên quan chặt chẽ đến phần lớn các trường hợp ung thư cổ tử cung 2.
Bộ gen HPV là DNA vòng, sợi kép, kích thước khoảng 7-8 kb, gồm ba vùng chức năng chính: vùng điều hoà thượng nguồn (URR), vùng gen sớm (E) và vùng gen muộn (L). Vùng URR chứa các yếu tố điều hoà phiên mã và vị trí gắn của protein E1 và E2, đóng vai trò trung tâm trong khởi phát sao chép và điều hoà biểu hiện gen virus, đồng thời cũng là vùng biến thiên cao nhất của bộ gen. Vùng gen sớm mã hoá các protein E1, E2, E4, E5, E6, E7 và E8, tham gia vào quá trình sao chép virus và điều hoà chu kỳ tế bào chủ, trong khi vùng gen muộn mã hoá hai protein cấu trúc L1 và L2 cần thiết cho quá trình lắp ráp virion 3.
HPV xâm nhập vào lớp tế bào đáy của biểu mô thông qua các vi tổn thương, bám vào heparan sulfate proteoglycan và các thụ thể thứ cấp như α6-integrin, từ đó đi vào tế bào qua cơ chế nhập bào. Bộ gen virus được vận chuyển vào nhân trong quá trình phân bào và tồn tại dưới dạng episome. Ở giai đoạn nhiễm sớm và duy trì, HPV chủ yếu biểu hiện các protein E1 và E2 nhằm khởi động sao chép DNA virus và duy trì số lượng bản sao thấp, giúp virus tồn tại dai dẳng và tránh sự nhận diện của hệ miễn dịch.
Đối với hr-HPV, đặc biệt là HPV-16 và HPV-18, virus có khả năng thúc đẩy tăng sinh tế bào biểu mô đáy và cận đáy, tạo điều kiện cho nhiễm kéo dài. Khi tế bào biểu mô biệt hoá, virus khai thác đáp ứng tổn thương DNA (DNA damage response, DDR) của tế bào chủ để khuếch đại bộ gen, làm gia tăng nguy cơ tích hợp DNA HPV vào bộ gen tế bào. Sự tích hợp này thường dẫn bất hoạt hoặc gián đoạn gen E2, dẫn đến tăng biểu hiện kéo dài hai oncoprotein E6 và E7. Protein E6 thúc đẩy thoái hóa p53, trong khi E7 bất hoạt protein pRb, từ đó gây rối loạn kiểm soát chu kỳ tế bào, ức chế chết theo chương trình và thúc đẩy tích lũy tổn thương hệ gen. Song song đó, hr-HPV còn gây suy giảm đáp ứng miễn dịch và rối loạn điều hoà biểu sinh, tạo điều kiện cho sự hình thành và phát triển của các tổn thương, những biến đổi này là nền tảng cho sự hình thành tiền ung thư cổ tử cung (Cervical intraepithelial neoplasia – CIN) và tiến triển ung thư cổ tử cung 3,4.
Nhiều nghiên cứu cho thấy hệ vi sinh vật dọc theo đường sinh dục nữ vừa có những đặc điểm tương đồng, vừa tồn tại sự khác biệt rõ rệt khi di chuyển từ âm đạo lên cổ tử cung, nội mạc tử cung (NMTC), vòi trứng và dịch phúc mạc. Trong bối cảnh đó, thuật ngữ “hệ vi sinh cổ tử cung – âm đạo” (cervico-vaginal microbiota – CVM) được sử dụng để mô tả tập hợp các vi sinh vật cư trú tại âm đạo và cổ tử cung, bao gồm vi khuẩn, virus và nấm. Thành phần của CVM không cố định mà chịu ảnh hưởng bởi nhiều yếu tố như nội tiết, hoạt động tình dục, thói quen vệ sinh, cũng như việc sử dụng thuốc tránh thai và kháng sinh 4.
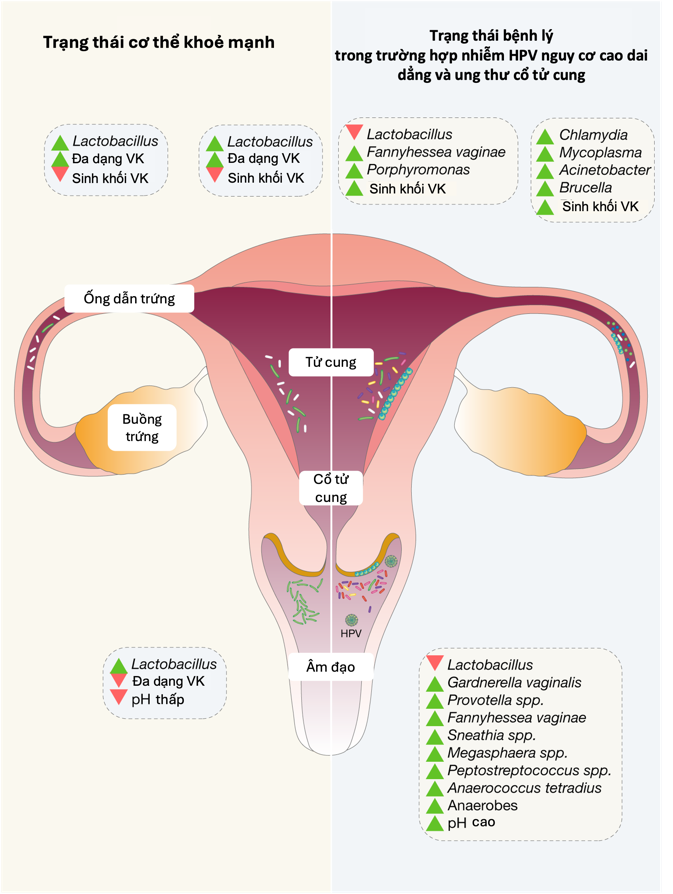
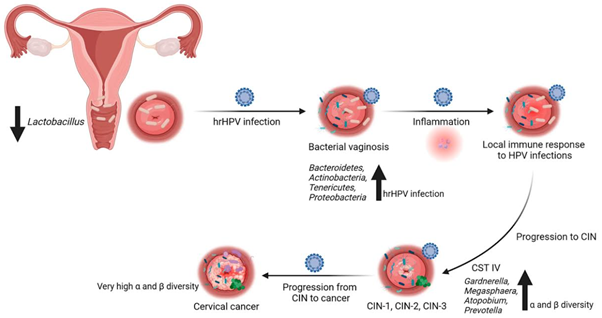
Hình 1. So sánh hệ vi sinh vật dọc theo đường sinh dục nữ trong trạng thái khỏe mạnh và trạng thái nhiễm HPV dai dẳng 1
Dựa trên thành phần vi khuẩn, CVM được phân loại thành các kiểu trạng thái khuẩn hệ (Community State Types – CSTs). Các CST giàu Lactobacillus (CST I, II, III và V) thường được xem là đặc trưng của trạng thái sinh lý khỏe mạnh. Cụ thể, CST I do L. crispatus chiếm ưu thế, CST II do L. gasseri, CST III do L. iners và CST V do L. jensenii. Các hệ vi sinh này góp phần duy trì môi trường âm đạo có pH thấp thông qua sản xuất axit lactic, từ đó ức chế sự phát triển của vi sinh vật gây hại, củng cố hàng rào niêm mạc và hỗ trợ đáp ứng miễn dịch tại chỗ. Ngược lại, CST IV đặc trưng bởi sự suy giảm đáng kể Lactobacillus và sự gia tăng của các vi khuẩn kỵ khí như Gardnerella, Atopobium, Prevotella và Megasphaera. Kiểu khuẩn hệ này thường liên quan đến tình trạng rối loạn vi sinh và nguy cơ mắc các bệnh lý. Đáng chú ý, sự phân bố các CST không hoàn toàn đồng nhất mà có thể khác nhau giữa các nhóm chủng tộc và sắc tộc 1,4.
Ngày càng có nhiều bằng chứng cho thấy tình trạng mất cân bằng hệ vi sinh cổ tử cung – âm đạo có liên quan đến nguy cơ nhiễm HPV dai dẳng, sự hình thành loạn sản cổ tử cung và tiến triển ung thư 5. Bên cạnh vai trò như một hàng rào sinh học, hệ vi sinh cổ tử cung – âm đạo còn tham gia điều hòa đáp ứng miễn dịch tại chỗ, từ đó ảnh hưởng đến khả năng đào thải hoặc tồn lưu HPV của vật chủ. Mặc dù việc triển khai rộng rãi tiêm vaccine HPV đã góp phần làm giảm đáng kể gánh nặng ung thư cổ tử cung, các chủng HPV không nằm trong phổ bảo vệ của vaccine vẫn tiếp tục gây nguy cơ nhiễm và bệnh lý liên quan. Hơn nữa, không phải tất cả các trường hợp nhiễm HPV đều tiến triển thành tổn thương tiền ung thư hay ung thư cổ tử cung. Theo Shen và cộng sự (2025), chỉ ra rằng yếu tố then chốt quyết định tiến triển bệnh không phải là sự lây nhiễm ban đầu mà là khả năng tồn tại dai dẳng của HPV trong biểu mô cổ tử cung 6. Quá trình này được điều hòa bởi sự tương tác phức tạp giữa đặc điểm sinh học của virus, đáp ứng miễn dịch của vật chủ và vi môi trường tại chỗ, trong đó hệ vi sinh vật âm đạo đóng vai trò trung tâm. Những phát hiện này nhấn mạnh tầm quan trọng của vi môi trường cổ tử cung – âm đạo như một yếu tố điều hoà với kết cục sinh học của nhiễm HPV.
Bên cạnh đó, sự hiện diện và số lượng Lactobacillus trong hệ vi sinh âm đạo thay đổi theo độ tuổi và chịu ảnh hưởng bởi nồng độ estrogen. Ở phụ nữ trong độ tuổi sinh sản, estrogen kích thích tích luỹ glycogen trong biểu mô âm đạo, Lactobacillus chuyển hóa glycogen biểu mô thành axit lactic, giúp duy trì pH thấp và hình thành hàng rào bảo vệ chống lại sự xâm nhập của vi sinh vật gây bệnh 7. Ngược lại, trong giai đoạn mãn kinh, sự suy giảm estrogen dẫn đến giảm lượng glycogen biểu mô, kéo theo sự suy giảm Lactobacillus và gia tăng vi khuẩn kỵ khí, từ đó làm tăng nguy cơ rối loạn vi sinh và các bệnh lý liên quan 8.
-
ẢNH HƯỞNG CỦA HPV ĐỐI VỚI HỖ TRỢ SINH SẢN (HTSS)
Các bằng chứng hiện nay cho thấy nhiễm HPV có thể tác động tiêu cực đến hiệu quả các kỹ thuật HTSS, tuy nhiên mức độ ảnh hưởng và cơ chế liên quan vẫn chưa được xác định rõ ràng do chưa có sự nhất quán giữa các nghiên cứu9.
Ở mức độ dịch tễ học, một phân tích tổng hợp gồm 11 nghiên cứu với 15.450 phụ nữ cho thấy nhiễm HPV nguy cơ cao có mối liên quan đáng kể đến vô sinh nữ (OR 2,33; 95% CI 1,42–3,83; p = 0,0008), trong khi nhiễm HPV nói chung (bao gồm tất cả kiểu gen) chỉ thể hiện xu hướng tăng nguy cơ nhưng không có ý nghĩa thống kê 10. Điều này làm nổi bật vai trò tiềm tàng của các kiểu gen HPV nguy cơ cao trong suy giảm khả năng sinh sản.
Bên cạnh đó, dữ liệu mô học và dịch tễ cho thấy HPV có thể hiện diện tại nhiều vị trí dọc theo đường sinh dục nữ. DNA virus không chỉ được phát hiện ở cổ tử cung và âm đạo mà còn được phát hiện ở NMTC, niêm mạc ống dẫn trứng, biểu mô buồng trứng 11. Mặc dù vậy, ý nghĩa sinh học của sự hiện diện này vẫn cần được làm sáng tỏ. Theo nghiên cứu của Zullo và cộng sự (2023), ở những phụ nữ nhiễm HPV tại cổ tử cung, virus cũng được phát hiện ở các mô sinh sản khác: 61% mẫu tế bào hạt buồng trứng và 48% mẫu tế bào NMTC đều dương tính với HPV. Đáng chú ý, việc có hay không nhiễm HPV tại tế bào hạt không ảnh hưởng đáng kể đến tỷ lệ noãn trưởng thành, tỷ lệ thụ tinh, chất lượng phôi, động học phát triển phôi hay tỷ lệ trẻ sinh sống. Ngược lại, những phụ nữ có sự hiện diện HPV tại NMTC có tỷ lệ trẻ sinh sống trên mỗi chu kỳ TTTON thấp hơn so với nhóm không nhiễm (14,7% so với 42,8%). Dù vậy, sự chênh lệch chưa đạt ý nghĩa thống kê, có thể do số lượng cỡ mẫu còn hạn chế 12. Nhìn chung, các dữ liệu gợi ý rằng vị trí nhiễm HPV có thể đóng vai trò khác nhau trong kết quả điều trị HTSS và cần được xem xét trong đánh giá lâm sàng.
Ở mức độ phôi học, nhiễm HPV ở phụ nữ có thể liên quan đến thay đổi nhỏ trong động học phát triển của phôi. Nghiên cứu time-lapse của Zullo và cộng sự (2023) cho thấy phôi từ phụ nữ nhiễm HPV có xu hướng phân chia nhanh hơn ở giai đoạn sớm, thể hiện qua thời điểm hai tiền nhân biến mất (tPNf) và khoảng thời gian giữa lúc xuất hiện của hai tiền nhân và hai tiền nhân biến mất (tPNf-tPNa) rút ngắn hơn đáng kể (23,40 ± 2,64 so với 24,95 ± 5,39 giờ, p = 0,005). Tuy nhiên, tốc độ phát triển này lại chậm hơn khi phôi đạt đến giai đoạn phôi nang (tB) (15,51 ± 2,83 so với 17,40 ± 5,90 giờ, p = 0,014). Các quan sát này tương đồng với dữ liệu từ mô hình động vật. Mặc dù động học phát triển bị xáo trộn, những thay đổi này không đi kèm với khác biệt có ý nghĩa về chất lượng hình thái phôi, tỷ lệ thụ tinh hay tỷ lệ trẻ sinh sống 12.
Bên cạnh tác động lên phôi, các nghiên cứu in vitro cho thấy tế bào lá nuôi mang bộ gen HPV16 có tỷ lệ apoptosis tăng, cho thấy khả năng rối loạn chức năng nhau thai và giảm khả năng xâm nhập của phôi. Điều này có thể góp phần giải thích mối liên quan giữa nhiễm HPV với nguy cơ sẩy thai sớm hoặc vỡ ối non trong một số báo cáo 13.
Tóm lại, mặc dù bằng chứng hiện tại vẫn chưa hoàn toàn nhất quán, nhưng các dữ liệu hiện có cho thấy nhiễm HPV – đặc biệt kiểu gen nguy cơ cao – có thể tác động tiêu cực đến khả năng sinh sản và kết quả HTSS thông qua tác động lên NMTC và động học phát triển phôi. Những phát hiện này nhấn mạnh tầm quan trọng của việc tầm soát và quản lý HPV ở phụ nữ trong độ tuổi sinh sản, đặc biệt ở nhóm điều trị HTSS, nhằm tối ưu hoá kết quả sinh sản và hạn chế các biến cố bất lợi.
-
TRIỂN VỌNG ĐIỀU TRỊ VÀ NGĂN NGỪA TỪ ĐIỀU CHỈNH HỆ VI SINH VẬT
Những hiểu biết hiện nay về hệ vi sinh cổ tử cung – âm đạo đã mở ra các hướng tiếp cận mới trong phòng ngừa và hỗ trợ điều trị các tổn thương liên quan đến HPV cũng như ung thư cổ tử cung. Ngày càng nhiều bằng chứng cho thấy trạng thái hệ vi sinh ưu thế Lactobacillus đóng vai trò quan trọng trong việc duy trì hàng rào bảo vệ niêm mạc, điều hoà đáp ứng miễn dịch tại chỗ và hạn chế sự tồn tại dai dẳng của HPV. Trên cơ sở đó, các chiến lược điều chỉnh hệ vi sinh, đặc biệt là tái lập môi trường âm đạo ưu thế Lactobacillus, được xem như một chiến lược sinh học tiềm năng nhằm hỗ trợ quá trình đào thải HPV và phục hồi cân bằng sinh lý niêm mạc cổ tử cung. Nhiều nghiên cứu tập trung vào vai trò của các chủng Lactobacillus như L. crispatus, L. jensenii, L. rhamnosus, L. reuteri và L. casei. Trong số đó, L. crispatus được đánh giá cao nhờ khả năng duy trì pH âm đạo ở mức axit ổn định thông qua sản xuất axit lactic, đồng thời ức chế sự tồn tại dai dẳng của virus. Việc sử dụng probiotics đường uống hoặc đặt âm đạo đã được ghi nhận có liên quan đến tăng tỷ lệ đào thải HPV, cải thiện bất thường tế bào học và kết quả soi cổ tử cung trong một số nghiên cứu lâm sàng 4, 14, 13. Tuy nhiên, phần lớn các bằng chứng hiện nay vẫn mang tính hỗ trợ và quan sát, chưa thể khẳng định chắc chắn mối tương quan giữa việc điều chỉnh hệ vi sinh vật và hiệu quả điều trị hoặc phòng ngừa các tổn thương liên quan đến HPV. Theo đó, các thử nghiệm lâm sàng ngẫu nhiên có đối chứng và được thiết kế chặt chẽ hơn vẫn cần thiết để làm rõ vai trò thực sự của các can thiệp điều chỉnh hệ vi sinh.
-
KẾT LUẬN
Các bằng chứng hiện nay cho thấy hệ vi sinh cổ tử cung – âm đạo đóng vai trò quan trọng trong điều hòa nguy cơ nhiễm và tồn tại dai dẳng của HPV thông qua ảnh hưởng lên pH, hàng rào niêm mạc và miễn dịch tại chỗ. Môi trường ưu thế Lactobacillus giúp tăng khả năng đào thải HPV, trong khi kiểu hệ vi sinh nghèo Lactobacillus liên quan đến viêm mạn tính và nguy cơ tiến triển tổn thương cổ tử cung.
Song song đó, HPV có thể tác động đến một số khía cạnh của HTSS như sự làm tổ, động học phát triển của phôi và chức năng NMTC, dù bằng chứng hiện tại chưa thống nhất và chưa xác định được quan hệ nhân quả rõ ràng.
Nhìn chung, HPV nhiều khả năng không phải là yếu tố nguy cơ đơn lẻ, mà đóng vai trò điều biến trong bối cảnh vi môi trường vi sinh – miễn dịch của vật chủ. Các nghiên cứu tương lai cần tiếp cận tích hợp hệ vi sinh, kiểu gen HPV và đáp ứng miễn dịch để hiểu rõ hơn về cơ chế bệnh sinh và tối ưu hoá kết quả HTSS.
Tài liệu tham khảo
1. Bautista J, Altamirano-Colina A, López-Cortés A. The vaginal microbiome in HPV persistence and cervical cancer progression. Front Cell Infect Microbiol. 2025;15. doi:10.3389/fcimb.2025.1634251
2. Włoszek E, Krupa K, Skrok E, Budzik MP, Deptała A, Badowska-Kozakiewicz A. HPV and Cervical Cancer—Biology, Prevention, and Treatment Updates. Curr Oncol. 2025;32(3). doi:10.3390/curroncol32030122
3. Zhang Y, Qiu K, Ren J, Zhao Y, Cheng P. Roles of human papillomavirus in cancers: oncogenic mechanisms and clinical use. Signal Transduct Target Ther. 2025;10(1):44. doi:10.1038/s41392-024-02083-w
4. Głowienka-Stodolak M, Bagińska-Drabiuk K, Szubert S, et al. Human Papillomavirus Infections and the Role Played by Cervical and Cervico-Vaginal Microbiota-Evidence from Next-Generation Sequencing Studies. Cancers. 2024;16(2):399. doi:10.3390/cancers16020399
5. Cascardi E, Cazzato G, Daniele A, et al. Association between Cervical Microbiota and HPV: Could This Be the Key to Complete Cervical Cancer Eradication? Biology. 2022;11(8):1114. doi:10.3390/biology11081114
6. Shen S, Zhao S, Shan J, Ren Q. Metabolomic and microbiota profiles in cervicovaginal lavage fluid of women with high-risk human papillomavirus infection. Sci Rep. 2025;15(1):796. doi:10.1038/s41598-024-84796-0
7. Alizadehmohajer N, Shojaeifar S, Nedaeinia R, et al. Association between the microbiota and women’s cancers - Cause or consequences? Biomed Pharmacother Biomedecine Pharmacother. 2020;127:110203. doi:10.1016/j.biopha.2020.110203
8. Zhou ZW, Long HZ, Cheng Y, Luo HY, Wen DD, Gao LC. From Microbiome to Inflammation: The Key Drivers of Cervical Cancer. Front Microbiol. 2021;12. doi:10.3389/fmicb.2021.767931
9. Kristensen, T. S., Foldager, A., Laursen, A. S. D., & Mikkelsen, E. M. (2025). Sexually transmitted infections (Chlamydia trachomatis, genital HSV, and HPV) and female fertility: A scoping review. Sexual & Reproductive Healthcare, 101067.
10. Yuan S, Qiu Y, Xu Y, Wang H. Human papillomavirus infection and female infertility: a systematic review and meta-analysis. Reprod Biomed Online. 2020;40(2):229-237. doi:10.1016/j.rbmo.2019.10.019
11. Ardekani, A., Taherifard, E., Mollalo, A., Hemadi, E., Roshanshad, A., Fereidooni, R., Rouholamin, S., Rezaeinejad, M., Farid-Mojtahedi, M., Razavi, M., & Rostami, A. (2022). Human Papillomavirus Infection during Pregnancy and Childhood: A Comprehensive Review. Microorganisms, 10(10), 1932. https://doi.org/10.3390/microorganisms10101932.
12. Zullo F, Fiano V, Gillio-Tos A, et al. Human papillomavirus infection in women undergoing in-vitro fertilization: effects on embryo development kinetics and live birth rate. Reprod Biol Endocrinol RBE. 2023;21(1):39. doi:10.1186/s12958-023-01091-9
13. Li Y, Yu T, Yan H, et al. Vaginal Microbiota and HPV Infection: Novel Mechanistic Insights and Therapeutic Strategies. Infect Drug Resist. 2020;13:1213-1220. doi:10.2147/IDR.S210615
14. Mitra A, Gultekin M, Burney Ellis L, et al. Genital tract microbiota composition profiles and use of prebiotics and probiotics in gynaecological cancer prevention: review of the current evidence, the European Society of Gynaecological Oncology prevention committee statement. Lancet Microbe. 2024;5(3):e291-e300. doi:10.1016/S2666-5247(23)00257-4