NHS. Bùi Thị Huyền Trang, NHS. Nguyễn Hoàng Trân, TS.BS. Hồ Nguyễn Tường
Đơn vị Hỗ trợ sinh sản IVFMD - Bệnh viện Mỹ Đức
-
GIỚI THIỆU
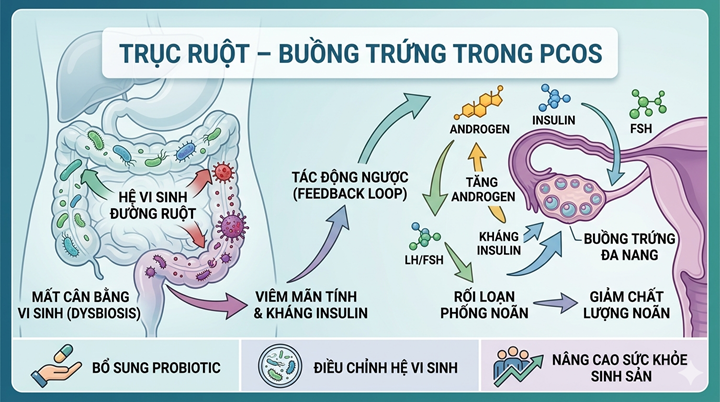
Hội chứng buồng trứng đa nang (HC BTĐN) là một rối loạn nội tiết và chuyển hóa hệ thống với các biểu hiện lâm sàng trải dài suốt chu kỳ sống của phụ nữ, từ giai đoạn dậy thì đến hậu mãn kinh. Bản chất bệnh lý của HC BTĐN bắt nguồn từ sự rối loạn điều hòa các tín hiệu nội tiết, dẫn đến tình trạng cường androgen và mất cân bằng hormone sinh dục. Vượt ra ngoài các rối loạn chức năng sinh sản đơn thuần, HC BTĐN còn liên quan chặt chẽ đến các bệnh lý chuyển hóa, đặc biệt là đề kháng insulin (Insulin Resistance - IR), béo phì và gia tăng nguy cơ bệnh lý tim mạch. Trong những năm gần đây, sự phát triển của công nghệ giải trình tự gen thế hệ mới đã định nghĩa lại quan điểm về cơ chế bệnh sinh của HC BTĐN, dịch chuyển trọng tâm từ các trục nội tiết truyền thống sang trục Ruột – Buồng trứng (Gut–Ovary Axis). Các bằng chứng thực nghiệm và lâm sàng ngày càng củng cố giả thuyết rằng sự mất cân bằng hệ vi sinh đường ruột không đơn thuần là hệ quả thứ phát của lối sống, mà đóng vai trò là tác nhân khởi phát then chốt thúc đẩy diễn tiến bệnh. Bài viết này tập trung phân tích các cơ chế tương tác phức tạp giữa hệ vi sinh và các rối loạn nội tiết – chuyển hóa, đồng thời thảo luận về triển vọng của các liệu pháp điều chỉnh cân bằng vi sinh trong quản lý và điều trị HC BTĐN toàn diện.
-
ĐẶC ĐIỂM HỆ VI SINH Ở PHỤ NỮ MẮC HC BTĐN
Hệ vi sinh ở phụ nữ có chẩn đoán HC BTĐN là một bức tranh phức tạp về sự thay đổi đa dạng sinh học và thành phần các chủng vi khuẩn so với nhóm phụ nữ không mắc phải hội chứng này, thể hiện rõ nét qua tình trạng mất cân bằng ở nhiều khoang cơ thể khác nhau, đặc biệt là đường ruột và hệ sinh dục. Hệ vi sinh này, thường được gọi là “cơ quan thứ hai’’ hay “bộ gen thứ hai’’ của con người, đóng vai trò quan trọng trong việc duy trì cân bằng nội mô, nhưng ở phụ nữ HC BTĐN, hệ vi sinh này bộc lộ những biến đổi đặc trưng cả về số lượng, chất lượng và chủng loại.
2.1 Hệ vi sinh đường ruột
Sự suy giảm đa dạng sinh học
Đặc diểm nổi bật đầu tiên trong hệ vi sinh đường ruột của phụ nữ HC BTĐN là sự sụt giảm đáng kể về độ đa dạng sinh học. Các chỉ số đa dạng alpha (độ phong phú và đồng đều của các loại trong cùng một mẫu) và đa dạng beta (sự khác biệt về thành phần loài giữa các cá thể) đều thấp hơn rõ rệt so với phụ nữ khoẻ mạnh [1]. Sự suy giảm tính đa dạng này không mang tính ngẫu nhiên mà được quan sát thấy có mối tương quan nghịch với nồng độ androgen trong máu, tổng lượng testosterone và tình trạng rậm lông trên lâm sàng. Điều này có nghĩa là mức độ mất cân bằng của hệ sinh thái vi khuẩn càng nghiêm trọng thì các biểu hiện nội tiết nam tính hoá càng rõ rệt [2].
Về mặt cấu trúc ở cấp độ ngành, hệ vi sinh đường ruột ở phụ nữ HC BTĐN ghi nhận sự thay đổi lớn về tỷ lệ giữa các nhóm vi khuẩn chủ chốt. Cụ thể nghiên cứu đã chỉ ra sự gia tăng tỷ lệ Bacteroidetes so với Firmicutes. Trong khi người bình thường, hai ngành ngày duy trì một sự cân bằng nhất định để hỗ trợ chuyển hoá năng lượng thì ở phụ nữ HC BTĐN sự bùng phát của Bacteroidetes và sự suy giảm của Firmicutes tạo nên một môi trường vi sinh vật khác biệt hoàn toàn [3][4].
Sự ‘’đổi ngôi’’ giữa lợi khuẩn và tác nhân gây viêm
Đi sâu vào cấp độ chi và loài, sự biến đổi thành phần vi khuẩn đường ruột ở phụ nữ HC BTĐN cho thấy một sự "đổi ngôi" giữa các lợi khuẩn và các tác nhân gây viêm. Những ‘’vệ sĩ’’ quan trọng như Akkermansia muciniphila vốn có vai trò bảo vệ lớp chất nhầy niêm mạc hay các chi Lactobacillus và Bifidobacterium hỗ trợ miễn dịch, đều bị sụt giảm nghiêm trọng. Bên cạnh đó, Faecalibacterium prausnitzii và Roseburia được chứng minh có khả năng sản xuất các axit béo chuỗi ngắn có lợi, nhưng ở phụ nữ HC BTĐN, số lượng của các loài này bị suy giảm đáng kể. Thay vào đó là sự bùng phát của vi khuẩn Gram âm như Bacteroides vulgatus, Escherichia và Shigella. Các chủng này sở hữu lớp vỏ nội độc tố (Lipopolysaccharide - LPS), biến đường ruột thành một ‘’kho chứa’’ nội độc tố khổng lồ [5].
Bên cạnh những thay đổi về thành phần loài, đặc điểm cân bằng vi sinh ở phụ nữ HC BTĐN còn thể hiện qua sự biến đổi các sản phẩm chuyển hoá vi khuẩn. Hệ vi sinh vật ở những phụ nữ này có sự thiếu hụt các axit béo chuỗi ngắn (Short-chain fatty acids - SCFAs) đặc biệt là butyrate và propionate. Nồng độ các chất này trong phân và máu của người được chẩn đoán HC BTĐN thấp hơn hẳn người bình thường do các chủng vi khuẩn sản xuất chúng bị tiêu diệt hoặc ức chế [6]. Sự làm giàu các gen mã hóa enzym thủy phân muối mật (Bile Salt Hydrolases - BSH) đã gây ra rối loạn chuyển hóa axit mật, làm xáo trộn nồng độ các axit mật sơ cấp và thứ cấp trong dịch nang cũng như máu, đặc biệt là sự gia tăng các axit mật liên hợp như glycocholic acid và taurocholic acid [7].
Hệ vi sinh ở phụ nữ HC BTĐN có xu hướng ưu tiên các con đường chuyển hóa axit amin, dẫn đến nồng độ các axit amin chuỗi nhánh (Branched-chain amino acids - BCAAs)như leucine, valine và isoleicine tăng cao vượt mức trong huyết thanh và dịch nang [8].
2.2 Hệ vi sinh đường sinh dục (Âm đạo và tử cung)
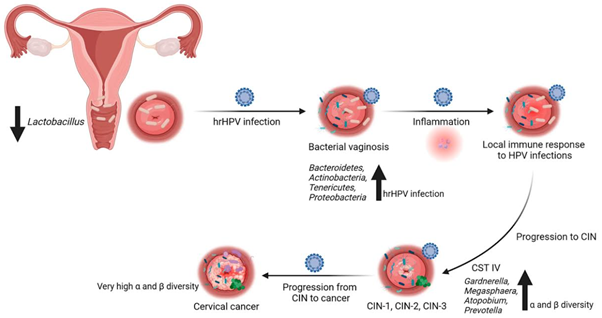
Tại hệ sinh dục, đặc điểm cân bằng vi sinh âm đạo của phụ nữ HC BTĐN cũng có những xáo trộn đặc trưng không kém đường ruột. Ở phụ nữ khỏe mạnh, hệ vi sinh này thường bị chiếm ưu thế tuyệt đối bởi các loài thuộc chi Lactobacillus (như L. crispatus, L. gasseri, L. iners) để duy trì môi trường axit ngăn chặn các tác nhân gây hại. Tuy nhiên, ở bệnh nhân HC BTĐN, "hàng rào" này bị sụp đổ, nhường chỗ cho sự bùng phát của các vi khuẩn kỵ khí như Gardnerella vaginalis, Prevotella và Sneathia, đẩy hệ sinh thái vào trạng thái CST IV (Community State Type IV) - một trạng thái đa dạng về chủng loại nhưng thiếu hụt vi khuẩn bảo vệ, tạo ra môi trường dễ bị viêm nhiễm và ảnh hưởng trực tiếp đến chức năng sinh sản của phụ nữ [9][10].
Ngoài ra, các nghiên cứu còn ghi nhận sự khác biệt về đặc điểm vi sinh giữa các thể lâm sàng của HC BTĐN. Ví dụ, phụ nữ HC BTĐN có kèm theo béo phì thường có mức độ sụt giảm lợi khuẩn Lactobacillus và Bifidobacterium nghiêm trọng hơn, đồng thời có sự gia tăng mạnh hơn của họ vi khuẩn đường ruột Enterobacteriaceae so với những bệnh nhân HC BTĐN có thể trạng gầy. Ở những bệnh nhân HC BTĐN có kèm theo tình trạng đề kháng insulin, hệ vi sinh âm đạo lại bộc lộ sự khác biệt rõ rệt ở các chi Ruminococcaceae và Lachnospiraceae so với nhóm không có kháng insulin [9][11].
Tóm lại, đặc điểm cân bằng hệ vi sinh ở phụ nữ HC BTĐN là một trạng thái mất cân bằng đa hệ thống, đặc trưng bởi sự suy tàn của các chủng vốn có vai trò thường trú tại chỗ (Akkermansia, Lactobacillus, Bifidobacterium) và sự lên ngôi của các chủng vi khuẩn Gram âm sinh độc tố cùng nhóm vi khuẩn kỵ khí gây bệnh. Hệ sinh thái này không còn giữ được chức năng điều hòa chuyển hóa và bảo vệ như bình thường, mà thay vào đó là một hệ vi sinh nghèo nàn về chủng loại nhưng lại giàu các thành phần gây rối loạn nội môi. Sự biến đổi này diễn ra cả ở đường tiêu hóa đến đường sinh dục kế cận, tạo nên môi trường vi sinh đặc thù ở phụ nữ được chẩn đoán mắc phải hội chứng HC BTĐN.
3. ẢNH HƯỞNG CỦA SỰ MẤT CÂN BẰNG HỆ VI SINH Ở PHỤ NỮ ĐƯỢC CHẨN ĐOÁN HC BTĐN
Sự mất cân bằng hệ vi sinh ở phụ nữ HC BTĐN không chỉ là một dấu hiệu của hội chứng này mà đã được chứng minh có thể đóng vai trò then chốt trong cơ chế bệnh sinh. Tác động của sự mất cân bằng này có thể được giải thích thông qua một mạng lưới tương tác phức tạp giữa nội tiết, miễn dịch và chức năng sinh sản. Dưới đây là góc nhìn đa chiều về cơ chế ảnh hưởng của sự mất cân bằng hệ vi sinh trong HC BTĐN:
3.1 Vòng xoắn giữa kháng Insulin và tăng androgen
Thay đổi môi trường vi sinh có thể ảnh hưởng đến sự điều hòa nội tiết và chuyển hóa của cơ thể. Sự xáo trộn quần thể vi sinh đường ruột khởi đầu cho sự phá vỡ tính toàn vẹn của hàng rào biểu mô, dẫn đến tình trạng nhiễm độc nội độc tố (Lipopolysaccharide - LPS) chuyển hóa. Việc giải phóng nội độc tố Lipopolysaccharide từ các vi khuẩn Gram âm vào hệ tuần hoàn kích hoạt thụ thể TLR4 (Toll-Like Receptor 4). Tình trạng này làm rối loạn chức năng thụ thể insulin, gây ra kháng insulin – yếu tố trung tâm của HC BTĐN ảnh hưởng đến 50-70% bệnh nhân [12,13,14].
Tình trạng kháng insulin này, kết hợp với sự sụt giảm các chất chuyển hóa có lợi như axit béo chuỗi ngắn và rối loạn chuyển hóa axit mật, tạo thành một "vòng xoắn" nội tiết bất lợi. Nồng độ insulin cao trong máu phối hợp cùng hormone LH kích thích trực tiếp tế bào vỏ buồng trứng sản xuất quá mức androgen. Vi khuẩn còn có thể có khả năng tham gia trực tiếp vào chuyển hóa hormone. Ví dụ, vi khuẩn Clostridium scindens sở hữu enzyme có thể chuyển đổi glucocorticoid thành androgen. Ngoài ra, một số chủng Pseudomonas có thể tiết ra sulfatase để chuyển đổi dạng không hoạt động (Dehydroepiandrosterone Sulfate - DHEAS) thành dạng hoạt động (Dehydroepiandrosterone – DHEA), làm trầm trọng thêm tình trạng dư thừa nội tiết nam. Đồng thời, sự gia tăng các cytokine gây viêm như IL-6 còn thúc đẩy biểu hiện gen CYP17A1, làm trầm trọng thêm tình trạng cường androgen hệ thống – tác nhân chính gây ra các triệu chứng rậm lông, mụn trứng cá và rối loạn phóng noãn [2].
3.2 Tình trạng viêm mãn tính cấp độ thấp
Sự mất cân bằng vi sinh đóng vai trò như một "ngòi nổ" khởi phát cho các phản ứng miễn dịch bất lợi thông qua việc phá vỡ tính toàn vẹn của hàng rào ruột, tạo điều kiện cho nội độc tố và các mảnh vụn vi khuẩn xâm nhập hệ tuần hoàn [3][12].
Việc giải phóng liên tục các cytokine gây viêm (TNF-α, IL-6, IL-1) không chỉ củng cố tình trạng kháng insulin mà còn gây tổn thương vi môi trường tại buồng trứng. Tình trạng viêm mãn tính này không chỉ làm trầm trọng thêm tình trạng kháng insulin mà còn trực tiếp gây tổn thương các tế bào hạt trong buồng trứng, ảnh hưởng đến quá trình phát triển của nang noãn [2][3].
3.3 Rối loạn phóng noãn và chất lượng phôi
Sự mất cân bằng hệ vi sinh tại cả đường ruột và đường sinh dục tác động trực tiếp và đa diện đến khả năng sinh sản của phụ nữ HC BTĐN. Ở cấp độ hệ thống, tình trạng tăng androgen và kháng insulin do mất cân bằng hệ vi sinh làm gián đoạn trục Hạ đồi - Tuyến yên - Buồng trứng, gây ra tình trạng vô kinh hoặc kinh nguyệt không đều do không có sự phóng noãn [15][16]. Tại môi trường vi mô nang noãn, kháng insulin gây rối loạn năng lượng tại nang noãn, làm tăng quá trình đường phân và ức chế chu trình TCA (Tricarboxylic Acid Cycle), dẫn đến chất lượng noãn kém và tỷ lệ thụ thai thấp trong hỗ trợ sinh sản [2].
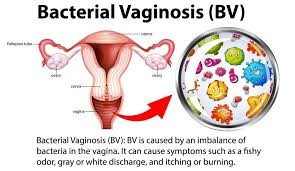
Bên cạnh đó, khả năng tiếp nhận của nội mạc tử cung cũng bị ảnh hưởng tiêu cực do sự sụt giảm biểu hiện của protein vận chuyển glucose GLUT4 (Glucose Transporter Type 4) dưới tác động của kháng insulin, tạo ra môi trường bất lợi cho sự làm tổ của phôi. Đặc biệt, sự mất cân bằng vi sinh tại đường sinh dục dưới — đặc trưng bởi sự sụt giảm quần thể Lactobacillus và sự trỗi dậy của các tác nhân gây bệnh như Gardnerella vaginalis và Prevotella — không chỉ làm tăng nguy cơ viêm âm đạo vi khuẩn (Bacterial Vaginosis - BV) mà còn liên quan mật thiết đến các kết cục thai kỳ bất lợi như chuyển phôi thất bại, sẩy thai liên tiếp và sinh non [16].
Tóm lại, theo giả thuyết DOGMA (Dysbiosis of Gut Microbiota), sự mất cân bằng hệ vi sinh khởi đầu một chuỗi các sự kiện: từ viêm hệ thống và kháng insulin đến rối loạn nội tiết androgen, cuối cùng dẫn đến những khiếm khuyết trong chức năng sinh sản và các biến đổi hình thái buồng trứng đa nang. Điều này cho thấy việc điều chỉnh hệ vi sinh là một hướng tiếp cận triển vọng trong điều trị toàn diện HC BTĐN.
4. TIỀM NĂNG CỦA ĐIỀU CHỈNH SỰ MẤT CÂN BẰNG VI SINH LÊN THỰC TRẠNG BỆNH LÝ VÀ CHẤT LƯỢNG CUỘC SỐNG CỦA PHỤ NỮ MẮC HỘI CHỨNG BUỒNG TRỨNG ĐA NANG
Việc ổn định và khôi phục trạng thái cân bằng vi sinh đang trở thành một hướng tiếp cận đầy triển vọng trong y học sinh sản, giúp phá vỡ các mắt xích bệnh lý phức tạp của HC BTĐN. Các can thiệp mục tiêu vào hệ vi sinh không chỉ cải thiện các chỉ số chuyển hóa mà còn tái cấu trúc môi trường nội tiết và nâng cao chất lượng cuộc sống cho bệnh nhân.
4.1 Tối ưu hóa chuyển hóa và kiểm soát kháng Insulin
Việc bổ sung Probiotic và Synbiotic đã được chứng minh lâm sàng giúp giảm đáng kể chỉ số HOMA-IR (Homeostasis Model Assessment of Insulin Resistance) và nồng độ insulin lúc đói [12][14]. Cơ chế này chủ yếu thông qua việc tăng cường các vi khuẩn sản xuất axit béo chuỗi ngắn (Short-chain fatty acids - SCFAs) như Akkermansia và Bifidobacterium, từ đó kích thích tiết hormone đường ruột GLP-1 (Glucagon-Like Peptide-1), cải thiện độ nhạy insulin và hỗ trợ giảm chỉ số BMI [3].
4.2 Tái thiết lập cân bằng nội tiết và giảm nồng độ androgen
Các can thiệp vi sinh vật mục tiêu, đặc biệt là các công thức đa chủng, đã ghi nhận khả năng làm giảm nồng độ testosterone tổng và chỉ số androgen tự do (Free Androgen Index - FAI) [24, 40]. Bằng cách điều chỉnh hệ vi sinh đường ruột, nồng độ hormone LH và tỷ lệ LH/FSH — những chỉ dấu thường bị nhiễu loạn trong HC BTĐN — dần được đưa về trạng thái sinh lý bình thường. Ngoài ra, sự gia tăng nồng độ globulin vận chuyển hormone sinh dục (Sex Hormone - Binding Globulin - SHBG) sau can thiệp giúp gắn kết và giảm lượng testosterone tự do, từ đó cải thiện các triệu chứng lâm sàng như rậm lông và mụn trứng cá [2].
4.3 Khôi phục chức năng phóng noãn và sức khỏe sinh sản
Sự cân bằng vi sinh tại cả đường ruột và đường sinh dục dưới đóng vai trò quyết định đến khả năng thụ thai. Các liệu pháp như bổ sung lợi khuẩn hoặc cấy ghép vi sinh vật đường ruột (Fecal Microbiota Transplantation - FMT) đã cho thấy tiềm năng trong việc phục hồi chu kỳ kinh nguyệt đều đặn và chức năng phóng noãn [11]. Trong một nghiên cứu thực hiện bởi Kaur và cộng sự, sử dụng lợi khuẩn đa chủng (Lactobacillus acidophilus UBLA-34, L. rhamnosus UBLR-58, L. reuteri UBLRu-87 , L. plantarum UBLP-40, L. casei UBLC-42, L. fermentum UBLF-31, Bifidobacterium bifidum UBBB-55) trong 6 tháng làm cải thiện có ý nghĩa thống kê tình trạng phóng noãn và kinh nguyệt. Trong hỗ trợ sinh sản (In Vitro Fertilization - IVF), một hệ vi sinh âm đạo khỏe mạnh với ưu thế Lactobacillus giúp giảm thiểu tình trạng viêm nhiễm phụ khoa, tạo điều kiện tối ưu cho sự làm tổ của phôi và giảm nguy cơ sẩy thai sớm [17].
4.4 Kháng viêm và củng cố hàng rào bảo vệ sinh học
Ổn định hệ vi sinh giúp phục hồi tính toàn vẹn của các liên kết chặt tại niêm mạc ruột, ngăn chặn hiệu quả sự rò rỉ nội độc tố vào hệ tuần hoàn. Việc cắt đứt "nguồn tiếp tế" nội độc tố này làm sụt giảm rõ rệt các cytokine gây viêm hệ thống như TNF-α, IL-6 và hs-CRP [19]. Điều này không chỉ bảo vệ các tế bào hạt buồng trứng khỏi tổn thương oxy hóa mà còn giảm thiểu nguy cơ mắc các bệnh lý tim mạch và tiểu đường tuýp 2 dài hạn cho phụ nữ HC BTĐN [3][14].
4.5. Ứng dụng các phương pháp điều trị mới
Trong bối cảnh y học hiện đại, việc tác động vào hệ vi sinh đang trở thành một chiến lược then chốt trong quản lý toàn diện HC BTĐN. Theo các nghiên cứu về liệu pháp hiệp đồng, y học cổ truyền với các bài thuốc kinh điển như Lục Vị Địa Hoàng hay các chiết xuất thảo dược không chỉ hỗ trợ điều hòa nội tiết mà còn đóng vai trò là các tác nhân tiền sinh học. Cơ chế này giúp thúc đẩy sự phát triển của các lợi khuẩn như Lactobacillus và Bifidobacterium, từ đó điều chỉnh hiệu quả con đường sinh tổng hợp hormone steroid và giảm nồng độ androgen hệ thống [17][18].
Đặc biệt, cấy ghép vi sinh vật đường ruột đang nổi lên như một phương pháp đột phá trong việc tái cấu trúc hoàn toàn hệ sinh thái ruột vốn bị mất cân bằng ở bệnh nhân HC BTĐN. Khác với việc bổ sung Probiotics đơn chủng, cấy ghép vi sinh vật đường ruột hướng tới khôi phục sự đa dạng sinh học của quần thể vi sinh, giúp cải thiện nhạy cảm insulin và giảm tình trạng viêm mạn tính do nội độc tố của vi khuẩn ngoại lai gây ra [19][20].
5. KẾT LUẬN
Các bằng chứng khoa học ủng hộ rằng việc duy trì một hệ vi sinh khỏe mạnh - bao gồm cả trục ruột và đường sinh dục không chỉ giúp cải thiện các triệu chứng lâm sàng như rậm lông, mụn trứng cá mà còn là chiến lược dự phòng quan trọng. Điều này giúp bảo vệ phụ nữ mắc HC BTĐN khỏi các biến chứng chuyển hóa dài hạn như tiểu đường tuýp 2, bệnh lý tim mạch và nâng cao tỉ lệ thành công trong hỗ trợ sinh sản.
TÀI LIỆU THAM KHẢO
-
He Y, Jin X, Wang H, et al. The emerging role of the gut Microbiome in poly- cystic ovary syndrome. F&S Reviews. 2021;2(3):214–26.
-
Samir M, Glister C, Mattar D, Laird M, Knight PG. Follicular expression of pro- inflammatory cytokines tumour necrosis factor-α (TNFα), Interleukin 6 (IL6) and their receptors in cattle: TNFα, IL6 and macrophages suppress thecal androgen production in vitro. Reprod (Cambridge England). 2017;154(1):35– 49.
-
Liu R, Zhang C, Shi Y, et al. Dysbiosis of gut microbiota associated with clinical parameters in polycystic ovary syndrome. Front Microbiol.2017;8:324.
-
Sherman SB, Sarsour N, Salehi M, et al. Prenatal androgen exposure causes hypertension and gut microbiota dysbiosis. Gut Microbes. 2018;9(5):400–21.
-
He F, Li Y. The gut microbial composition in polycystic ovary syndrome with insulin resistance: findings from a normal-weight population. J Ovarian Res. 2021;14(1):50.
-
Thursby E, Juge N. Introduction to the human gut microbiota. Biochem J. 2017 May 16;474(11):1823-1836.
-
Qi X, Yun C, Sun L, et al. Gut microbiota-bile acid-interleukin-22 axis orches- trates polycystic ovary syndrome. Nat Med. 2019;25(8):1225–33.
-
Gojda J, Cahova M. Gut microbiota as the link between elevated BCAA serum levels and insulin resistance. Biomolecules. 2021;11(10):1414.
-
Chen, X., et al. (2023). Effect of transvaginal Lactobacillus supplementation on reversing lower genital tract dysbiosis and improving perinatal outcomes in PCOS patients after IVF-FET: a study protocol for a multicenter randomized controlled trial. Trials.
-
Chudzicka-Strugała, I., et al. (2024). Bacterial vaginosis (BV) and vaginal microbiome disorders in women suffering from polycystic ovary syndrome (PCOS). Diagnostics.
-
Ahmed, S. (2021). Types of vaginal microbiomes in PCOS affected females. Indian Journal of Obstetrics and Gynecology Research.
-
Desbonnet L, Garrett L, Clarke G, et al. The probiotic bifidobacteria infantis: an assessment of potential antidepressant properties in the rat. J Psychiatr Res. 2008;43(2):164–74.
-
Page M, Kell J, B D, Pretorius E. The role of Lipopolysaccharide-Induced cell signalling in chronic inflammation. Chronic Stress (Thousand Oaks Calif). 2022;6:24705470221076390.
-
Remellen K, Pearce K. Dysbiosis of gut microbiota (DOGMA)--a novel theory for the development of polycystic ovarian syndrome. Med Hypotheses. 2012;79(1):104–12.
-
Lu, W., et al. (2021). Changes in vaginal microbiome diversity in women with polycystic ovary syndrome. Frontiers in Cellular and Infection Microbiology.
-
Gu, Y., et al. (2022). Gut and Vaginal Microbiomes in PCOS: Implications for Women's Health. Frontiers in Endocrinology.
-
Baker JM, Al-Nakkash L, Herbst-Kralovetz MM. Estrogen-gut Microbiome axis: physiological and clinical implications. Maturitas. 2017;103:45–53.
-
Edwards DP. Regulation of signal transduction pathways by Estrogen and progesterone. Annu Rev Physiol. 2005;67:335–76.
-
Tabrizi R, Ostadmohammadi V, Akbari M, et al. The effects of probiotic supple- mentation on clinical symptom, weight loss, glycemic control, lipid and hor- monal profiles, biomarkers of inflammation, and oxidative stress in women with polycystic ovary syndrome: a systematic review and Meta-analysis of randomized controlled trials. Probiotics Antimicrob Proteins. 2022;14(1):1–14.
-
Torres PJ, Ho BS, Arroyo P, et al. Exposure to a healthy gut Microbiome protects against reproductive and metabolic dysregulation in a PCOS mouse model. Endocrinology. 2019;160(5):1193–204.